Neumotórax espontáneo y neumomediastino en neumonía por SARS-CoV-2: serie de casos
Cogollo-González, Marysabel1; Zamora-Posada, Marlyn1; Sanmiguel-Reyes, Catalina1; Rodríguez-Gallego, Juan Pablo2; Conde-Camacho, Rafael Enrique2
Cogollo-González, Marysabel1; Zamora-Posada, Marlyn1; Sanmiguel-Reyes, Catalina1; Rodríguez-Gallego, Juan Pablo2; Conde-Camacho, Rafael Enrique2
RESUMEN
PALABRAS CLAVE
Complicaciones, COVID-19, enfisema mediastinal, neumotórax, lesión pulmonar.Introducción
El neumotórax se define como la acumulación de aire en el espacio pleural que puede ocurrir sin eventos desencadenantes en una persona sin enfermedad pulmonar, denominado neumotórax espontáneo primario, o surgir como una complicación de una enfermedad pulmonar o trauma subyacente conocido como neumotórax secundario.1
En diciembre de 2019 se describieron varios casos de neumonía de etiología desconocida en Wuhan (China),2,3 cuyo desarrollo posteriormente fue explicado por la identificación de un nuevo coronavirus que se denominó SARS-CoV-2, y a la enfermedad desencadenada por el virus, COVID-19.4 Desde entonces, se han asociado diferentes complicaciones, que incluyen el síndrome de dificultad respiratoria aguda (SDRA), las coagulopatías, la insuficiencia renal y las alteraciones cardíacas y neurológicas.5
Respecto a las enfermedades por coronavirus registradas previamente, el neumotórax espontáneo ha sido descrito como una complicación del SDRA causado por el SARS-CoV-1, con una incidencia de 1.7% en pacientes hospitalizados,6 y su aparición constituye un factor de mal pronóstico en el síndrome respiratorio del Medio Oriente (MERS).7 El neumotórax asociado con la COVID-19 tiene una incidencia entre 0.56 y 2%,8-12 y dentro de los presuntos mecanismos fisiopatológicos se plantean los cambios estructurales en el parénquima pulmonar producidos por el virus que conducen a daño alveolar difuso (DAD), descamación evidente de neumocitos y formación de membranas hialinas.13,14 Lo anterior propicia el desarrollo de neumatoceles y predispone a la aparición del neumotórax en los diferentes estadíos de la enfermedad.15 Entre otros factores de riesgo se encuentran los que aumentan la presión intratorácica como el uso de la ventilación mecánica (VM) y la tos prolongada.8,16
Por otro lado, el neumomediastino puede deberse a una fuga de aire a través del espacio intersticial secundario al aumento de la presión.17 El DAD y la rotura alveolar conllevan a enfisema intersticial y extensión del aire a lo largo de la vaina broncoalveolar hasta el mediastino.4 Dentro de los eventos que contribuyen a su desarrollo, se describen el tabaquismo, el consumo de drogas ilícitas, la enfermedad pulmonar intersticial, las infecciones pulmonares y la realización de maniobras de Valsalva vigorosas.4,18
Los casos de neumonía por COVID-19 que cursan con neumotórax bilateral y neumomediastino durante su evolución son raros, y al momento existen pocos reportes en la literatura.4,19 Nuestro objetivo es describir una serie de casos de neumotórax espontáneo y neumomediastino en el contexto de neumonía por COVID-19.
Reporte de casos
Caso 1. Masculino de 59 años, sin comorbilidades o tabaquismo previo. Consultó por mialgias, tos seca, anosmia y fiebre. Los signos vitales en la primera consulta se encontraban normales, con reporte de la reacción en cadena de la polimerasa con transcripción reversa (RT-PCR) para SARS-CoV-2 positiva. Se consideró infección leve por COVID-19 y se indicó aislamiento en casa. Al noveno día de síntomas, reingresó a la institución por disnea súbita y dolor pleurítico derecho. Al examen físico con hipertensión, taquicardia, taquipnea y saturación arterial de oxígeno (SaO2) en 86%. Los paraclínicos de ingreso demostraban linfopenia (leucocitos 7,910/mm3, linfocitos 950/mm3 [12%]) y elevación de los marcadores de severidad: proteína C reactiva 7.11 mg/dL (< 5 mg/dL), dímero D (DD) 840 ng/mL (< 500 ng/mL), lactato deshidrogenasa (LDH) 441 U/L (85-227 U/L) y ferritina 717 ng/mL (12 a 200 ng/mL).
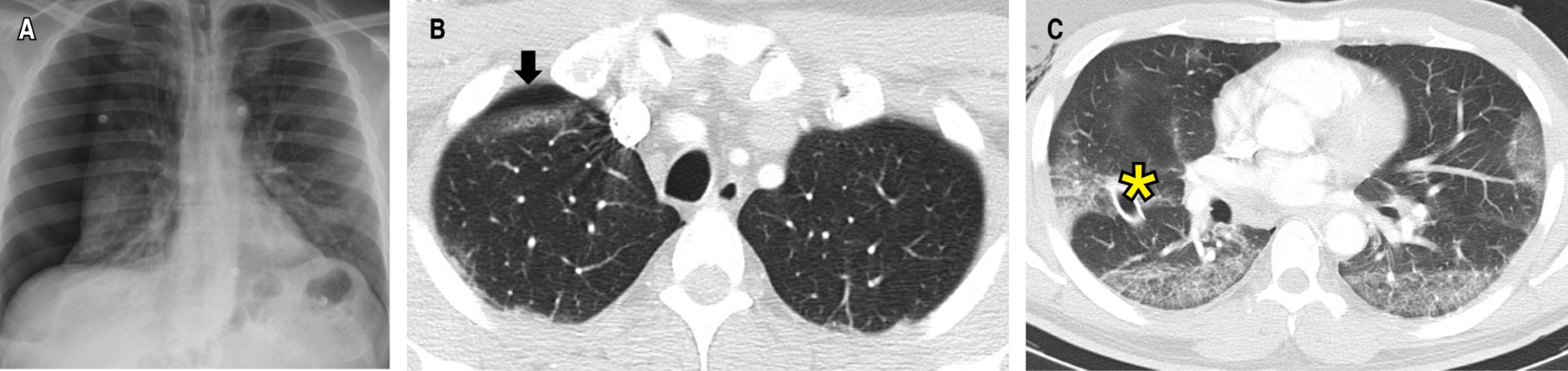
La radiografía de tórax demostró un neumotórax derecho con colapso de 50% del hemitórax ipsilateral (Figura 1A), que requirió manejo con toracostomía cerrada derecha y expansión completa pulmonar en los controles radiográficos. La angiotomografía (angio-TC) de tórax descartó tromboembolismo pulmonar (TEP) y evidenció opacidades en vidrio esmerilado (OVE) bilaterales, de distribución periférica, subpleural, con engrosamiento septal interlobulillar y enfisema subcutáneo derecho (Figuras 1By C). Se consideró neumonía por COVID-19, y su manejo consistió en dexametasona intravenosa (IV) de acuerdo al ensayo RECOVERY,20 oxígeno (FiO2 32%) y analgesia. A las 72 horas se retiró el tubo de tórax. Los laboratorios de control mostraron disminución de los marcadores de severidad, con egreso a los siete días de estancia hospitalaria. En el seguimiento a los tres meses (Tabla 1), la puntuación de la escala de disnea modificada del Medical Research Council (mMRC) fue de cero, sin alteraciones en las pruebas de función pulmonar, con OVE residuales en la tomografía control.
Caso 2. Masculino de 50 años, con antecedentes de hipertensión arterial (HTA) y sobrepeso, sin patologías respiratorias, tabaquismo o consumo previo de drogas ilícitas. Presentó infección moderada por SARS-CoV-2, con ingreso hospitalario para manejo con oxígeno por cánula nasal (FiO2 32%) y esteroide IV según el ensayo RECOVERY,20 con posterior egreso. En el día 20 desde el inicio de síntomas desarrolló disnea súbita y dolor retroesternal izquierdo, por lo que reconsultó a urgencias. Los signos vitales de ingreso mostraron taquicardia (120 latidos/minuto), taquipnea (26 respiraciones/minuto), y desaturación (SaO2 70%). Paraclínicos con leucocitosis (12,400/mm3), neutrofilia (10,500/mm3 [84.4%]), linfopenia (1,000/mm3 [8.08%]) y elevación de los marcadores de severidad: DD 990 ng/mL, LDH 408 U/L y ferritina 380 ng/mL.
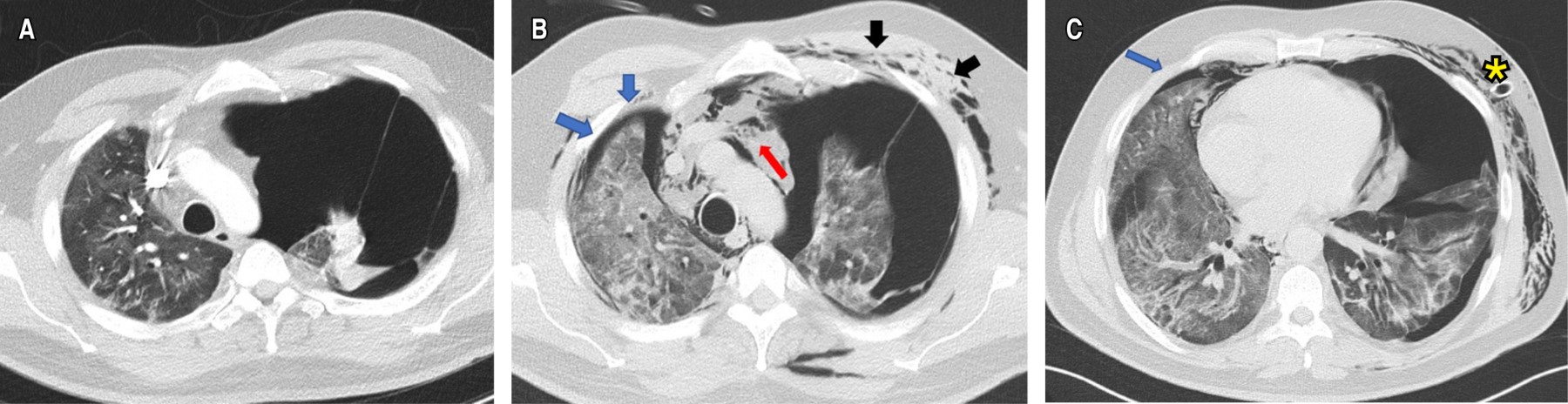
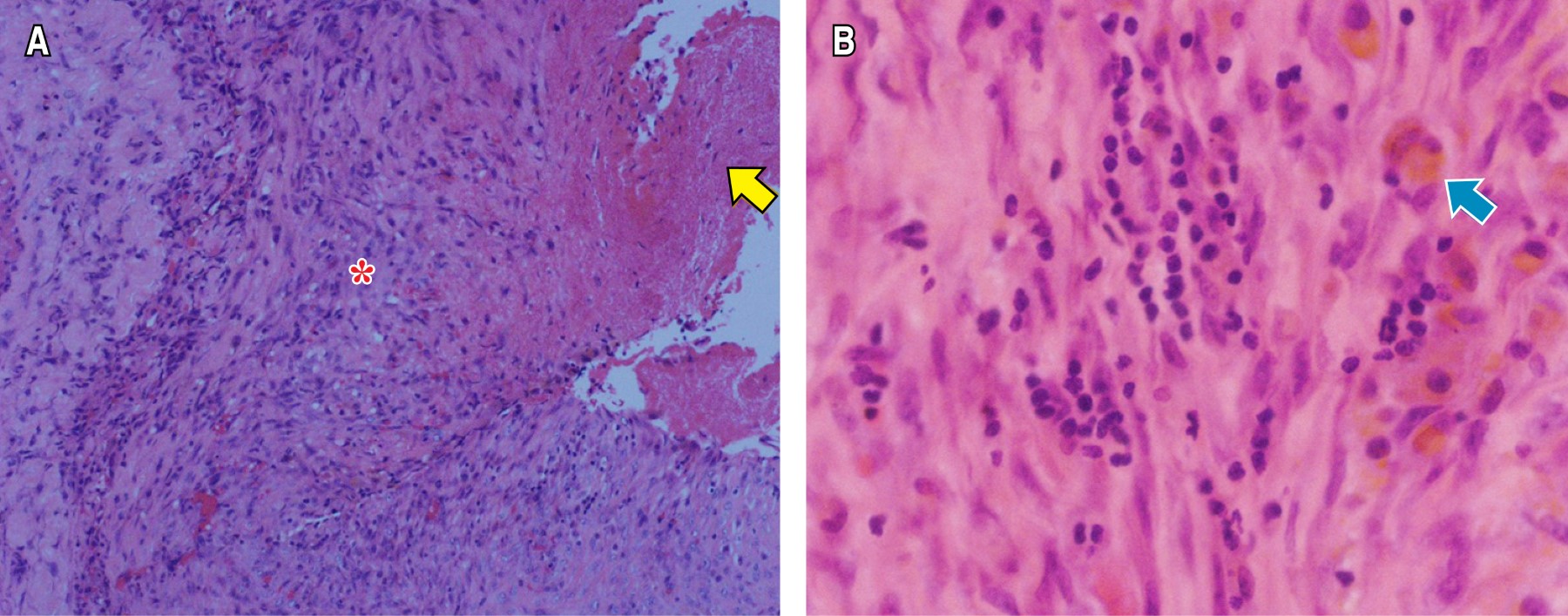
La angio-TC de tórax fue negativa para TEP, con evidencia de OVE del lado derecho y neumotórax contralateral que colapsaba 90% del pulmón (Figura 2A), por lo que se realizó una toracostomía cerrada izquierda de urgencia, sin lograrse la expansión pulmonar. Al tercer día de estancia hospitalaria, presentó deterioro de la oxigenación que requirió inicio de suplencia de oxígeno por cánula de alto flujo e ingresó a la unidad de cuidados intensivos (UCI) sin requerimiento de VM. La TC de alta resolución control (Figuras 2By C) demostró OVE, áreas de crazy paving de predomino derecho, neumotórax apical derecho pequeño (< 10%), neumomediastino y enfisema de los tejidos blandos del hemitórax izquierdo. Fue llevado a una segunda toracostomía cerrada a nivel apical izquierdo por cirugía de tórax, con persistencia del colapso pulmonar ipsilateral, por lo que se realizó decorticación y pleurectomía parietal por toracoscopia, con expansión satisfactoria. La patología reportó pleuritis crónica (Figura 3). Se indicó manejo conservador del neumotórax derecho, con expansión pulmonar en imágenes posteriores.
El reporte de imágenes previas en tórax aportado por el paciente no evidenciaba los hallazgos en el parénquima pulmonar durante esta hospitalización. Los estudios de autoinmunidad fueron negativos. Se consideró cuadro secundario a las complicaciones asociadas con neumonía severa por COVID-19. Por evolución favorable fue egresado a los 42 días de estancia hospitalaria. En la valoración a los 90 días (Tabla 1) se encontraba en rehabilitación pulmonar, continuaba con oxígeno a 1 L/min, refirió mejoría de la disnea, con una distancia recorrida por el test de caminata de seis minutos (TC6M) de 615 metros y un delta de SaO2 mayor de tres puntos. La TC control mostró lesión cicatricial en el lóbulo superior izquierdo por neumotórax y escasas OVE.
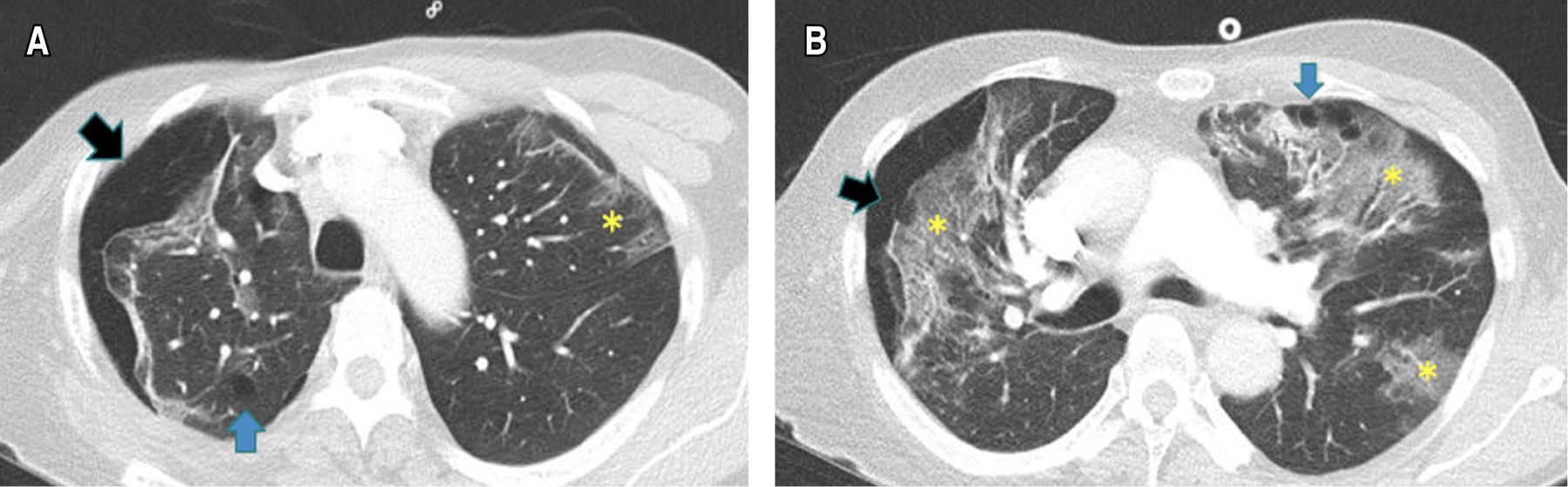
Caso 3. Masculino de 64 años, sin antecedentes relevantes ni tabaquismo. Ingreso hospitalario al día 11 de inicio de síntomas dados por disnea asociada a desaturación a medio ambiente (SaO2 85%), con confirmación molecular de infección por SARS-CoV-2 y radiografía de tórax con OVE difusas. El tratamiento inicial consistió en oxígeno (FiO2 32%), antipiréticos y dexametasona IV según el ensayo RECOVERY.20 Al día cuarto de estancia (día 15 de síntomas) presentó tos persistente, mayor deterioro del patrón respiratorio e hipoxemia severa sin mejoría con máscara de no reinhalación (FiO2 90%), ni pronación, además presencia de crepitaciones cervicales izquierdas. Paraclínicos con leucocitosis (16,600 cel/μL), linfopenia (300 cel/cel/μL), elevación de la LDH (524 U/L), hiperferritinemia (4,519 ng/mL) y DD en 630 ng/mL. Requirió intubación orotraqueal y traslado a la UCI. Se consideró descartar complicaciones de la COVID-19, se realizó una angio-TC de tórax que mostró TEP agudo y neumomediastino con enfisema cervical izquierdo (Figura 4). Se indicó anticoagulación con heparina de bajo peso molecular (1 mg por kg cada 12 horas), antibióticos y VM. Se realizaron otros estudios como fibrobroncoscopia y endoscopia de vías digestivas altas sin evidenciar hallazgos anormales. Se consideró neumomediastino espontáneo asociado a neumonía severa por SARS-CoV-2. Cirugía de tórax optó por manejo conservador, con una evolución hacia la mejoría y egreso al día 40. A los tres meses se realizaron pruebas de función pulmonar con espirometría sugestiva de restricción y capacidad de monóxido de carbono (DLCO), moderadamente disminuida (Tabla 1). En la actualidad continúa en sesiones de rehabilitación pulmonar con mejoría de la disnea.
Discusión
Los casos presentados describen pacientes con neumonía por COVID-19 sin antecedentes de enfermedades pulmonares, traumatismo torácico, VM o exposición significativa al tabaco, que desarrollaron neumotórax y/o neumomediastino espontáneo.
Según la serie de casos reportada por Martinelli et al. que evaluó 71 pacientes con infección por SARS-CoV-2, de los cuales 60 tuvieron neumotórax y 11 sólo neumomediastino, dentro de las características demográficas y clínicas más frecuentes se encuentran el sexo masculino, la edad de presentación entre 50 y 80 años, el compromiso unilateral del neumotórax (principalmente del lado derecho), la ausencia de hábito tabáquico y pocas comorbilidades médicas, siendo la más común la HTA.9 En relación con la fase de la enfermedad, se puede presentar al inicio, durante la hospitalización o de forma tardía.8,9 Wang y colaboradores reportaron un caso de infección por COVID-19 con neumotórax y neumomediastino de aparición en el día 20 de inicio de síntomas, de manera similar a nuestro segundo caso descrito.21
Los hallazgos imagenológicos distintivos de la neumonía por COVID-19 son OVE periféricas, subpleurales y bilaterales, que posteriormente progresan a consolidaciones, opacidades lineales, patrón de crazy paving y signo del "halo inverso". Lo anterior representa la correlación de los cambios tomográficos con la fisiopatología subyacente al proceso de la enfermedad a medida que se organiza.22 Diversos estudios han demostrado que en algunos pacientes con infección por COVID-19 hay progresión radiológica de áreas de consolidación a espacios aéreos anormales en la TC.16,23 Estos cambios quísticos redondos en la tomografía pueden estar asociados con el proceso de reabsorción de la consolidación, lo que podría explicarse por el daño causado a las paredes alveolares secundario a la infección, que conduce a neumatoceles e incrementa el riesgo de desarrollar neumotórax.24 Nuestros casos mostraron hallazgos radiológicos típicos de infección por COVID-19 con presencia de crazy paving en el segundo caso, que sugieren la relación temporal de los hallazgos imagenológicos y una evolución probablemente más tardía de la enfermedad.
La patología del segundo caso fue similar a lo documentado por Chang et al., quienes encontraron en algunos pacientes pleuritis crónica en muestras histopatológicas de pacientes llevados a cirugía torácica por complicaciones por COVID-19.25
La Tabla 2 resume las características clínicas y demográficas de algunos informes de casos de infección por SARS-CoV-2, donde se presentaron de manera simultánea neumotórax y neumomediastino, asociación infrecuente en la literatura.
El manejo de esta condición dependerá de la extensión del neumotórax y del estado general del paciente. En neumotórax parciales con estabilidad clínica se recomienda el manejo conservador y la vigilancia radiológica para descartar la progresión de esta entidad. En caso contrario, se indica la evacuación del aire mediante aspiración o drenaje.26 Los procedimientos en pleura pueden ser posibles generadores de aerosoles, por lo que los trabajadores de la salud deben hacer uso de todo el equipo de protección personal (EPP) y gestionar medidas para minimizar la propagación del virus durante la realización de estas intervenciones.27 En el estudio de Chang, ningún proveedor de atención médica fue positivo para COVID-19 después de las cirugías torácicas.25 En nuestros casos se utilizaron los EPP y se optó por manejo conservador y toracostomía cerrada como primera intervención quirúrgica. Ante la falta de respuesta al manejo inicial, se realizó decorticación y pleurectomía con todas las medidas de bioseguridad y en quirófano con presión negativa.
La persistencia de fuga de aire (de tres a cinco días) o la imposibilidad para lograr la expansión pulmonar son indicaciones de cirugía.26 La técnica quirúrgica se basa en la identificación y resección de áreas diana o ampollosas y una técnica de pleurodesis asociada, ya sea abrasión mecánica de la pleura parietal, pleurectomía química o apical.26,28 En la serie de casos por Chang, se describieron 13 pacientes con infección por COVID-19 sometidos a cirugías torácicas, dos por neumotórax y tres por neumatoceles.25 Aiolfi reportó dos pacientes con COVID-19 que fueron tratados exitosamente con pleurectomía por neumotórax persistente.29
El neumomediastino, en la mayoría de los casos, tiene un curso natural benigno con manejo conservador, que consiste en un estrecho seguimiento, reposo en cama, analgesia y oxigenoterapia.4 En nuestro caso, la evolución fue satisfactoria.
Nuestros pacientes tuvieron un seguimiento a los tres meses con mejoría de la sintomatología, en quienes necesitaron UCI se prescribió rehabilitación pulmonar y en el tercer caso se documentó alteración de la DLCO y espirometría sugestiva de restricción. Aunque hubo una buena distancia recorrida en el TC6M, en dos casos se observó un delta de SaO2 mayor de tres puntos durante la prueba. Los hallazgos imagenológicos mostraron mejoría y disminución de las lesiones en el tiempo.
Los estudios reportados a la fecha han sido de carácter observacional, lo cual impide establecer relaciones de causalidad entre el neumotórax, el neumomediastino y la infección por SARS-CoV-2. La serie de Martinelli et al. no evidenció que el neumotórax y el neumomediastino incrementaran la mortalidad a 28 días en los pacientes con COVID-19; sin embargo, la presencia de acidosis y la edad avanzada en ese contexto se relacionaron con una baja supervivencia.9 Recientemente, Miró et al. informaron que los pacientes con COVID-19 y neumotórax espontáneo tuvieron mayor riesgo de muerte intrahospitalaria en comparación con los dos grupos control (pacientes con COVID-19 sin neumotórax y aquéllos con neumotórax y sin infección por SARS-CoV-2). No obstante, los autores señalan que el tamaño muestral pequeño impide el ajuste de las variables vinculadas a la gravedad de la COVID-19.12 Por lo tanto, se requieren más estudios para determinar el pronóstico de estos pacientes.
La caracterización de los pacientes con estas complicaciones ofrece una orientación inicial que permite sugerir qué pacientes requieren un seguimiento más estricto, dado el riesgo de deterioro clínico y mortalidad. Esta serie de casos evidencia que su aparición no se limita a los pacientes críticamente enfermos y no sólo está determinada por la VM, sino que tal vez se explica por la fisiopatología de la enfermedad.
Conclusiones
La neumonía por SARS-CoV-2 puede presentar complicaciones en el curso de la enfermedad. Las principales causas son el TEP y la sobreinfección bacteriana; sin embargo, se deben considerar otros eventos infrecuentes como el neumotórax y/o neumomediastino, que pueden ser potencialmente fatales y ocurrir en pacientes sin antecedentes de traumatismo, tabaquismo o VM. Este grupo de pacientes en riesgo requeriría un seguimiento más estricto ante el riesgo de deterioro clínico y mortalidad. El mecanismo presuntivo es el DAD con posterior ruptura alveolar y formación de neumatoceles. En su manejo son importantes las medidas de protección por parte del personal de la salud para minimizar la aerolización.
Agradecimientos
A los pacientes y todo el personal de la Fundación Cardioinfantil-Instituto de Cardiología, Bogotá, Colombia.
AFILIACIONES
1Universidad de la Sabana, Cundinamarca, Colombia 2Fundación Cardioinfantil-Instituto de Cardiología y Fundación Neumológica Colombiana, Bogotá, Colombia.Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
REFERENCIAS
Hallifax R, Wrightson JM, Bibby A, Walker S, Stanton A, De Fonseca D, et al. Pleural services during the COVID-19 pandemic-revised. The British Thoracic Society. 2020. [Accessed Jan 18, 2021] Available in: www.brit-thoracic.org.uk/document-library/quality-improvement/covid-19/pleural-services-during-covid-19-pandemic/
|
Tabla 1: Seguimiento de los pacientes a los tres meses. |
|||||||
|
Caso |
Disnea mMRC* |
Oxígeno |
Espi- rometría |
DLCO ajustada a la altura |
TC6M (% de lo esperado) |
Rehabilitación pulmonar |
TCAR pulmonar control |
|
1 |
0 |
No |
Normal |
Normal (90%) |
617 m (92) ΔSaO2: -2% |
No |
Algunas OVE subpleurales residuales bilaterales y basales |
|
2 |
1 |
Sí (1 L/min) |
SD |
SD |
615 m (92) ΔSaO2: -9% |
Sí |
Lesión cicatrizal en LSI por neumotórax. Escasas OVE bilaterales |
|
3 |
2 |
No |
Sugestiva de restricción |
Moderadamente disminuida (55%) |
534 m (82) ΔSaO2: -7% |
Sí |
OVE residuales y bandas parenquimatosas bilaterales y basales. No neumomediastino |
|
*Escala de disnea modificada del Medical Research Council (mMRC). DLCO = capacidad de difusión de monóxido de carbono; TC6M = test de caminata de 6 minutos; TCAR = tomografía de alta resolución; ΔSaO2 = delta de saturación arterial de oxígeno; LSI = lóbulo superior izquierdo; OVE = opacidades en vidrio esmerilado; SD = sin datos. |
|||||||
|
Tabla 2: Resumen de casos de pacientes infectados por SARS-CoV-2 con neumomediastino y neumotórax. |
|||||||||
|
Autor |
País |
Casos |
Sexo / edad* |
Días de síntomas |
Tabaquismo- neumopatías |
VM previa |
Lado del neumotórax |
Manejo |
Desenlace |
|
Elhakim4 |
EE. UU. |
1 |
M/63 |
21 |
No |
No |
Bilateral |
Conservador |
Vivo |
|
Sonia5 |
EE. UU. |
1 |
M/62 |
12 |
No |
No |
Derecho |
Conservador |
Vivo |
|
Sun16 |
China |
1 |
M/38 |
15 |
No |
Sí, VMNI |
Izquierdo |
Conservador |
Vivo |
|
López19 |
España |
2 |
F/84 |
SD |
No |
No |
Bilateral |
SD |
Falleció |
|
|
|
|
M/67 |
5 |
No |
No |
Bilateral |
Tubo de tórax |
Falleció |
|
Wang21 |
China |
1 |
M/62 |
20 |
No |
No |
Derecho |
Conservador |
Vivo |
|
Shan30 |
China |
1 |
M/67 |
24 |
No |
No |
Derecho |
Conservador |
Vivo |
|
Quincho31 |
Perú |
1 |
F/55 |
7 |
Sí, asma |
No |
Derecho |
Conservador |
Falleció |
|
Oye32 |
EE. UU. |
2 |
M/32 |
SD |
No |
No |
Derecho |
Tubo de tórax, IOT |
SD |
|
|
|
|
F/56 |
SD |
No |
No |
Bilateral |
Tubo de tórax, IOT |
SD |
|
Eperjesiova33 |
EE. UU. |
1 |
SD |
SD |
No |
No |
Izquierdo |
Tubo de tórax |
SD |
|
Selvaraj34 |
EE. UU. |
1 |
M/77 |
3 |
No |
Sí, BPAP |
Bilateral |
Tubo de tórax |
Falleció |
|
Hazariwala35 |
EE. UU. |
1 |
F/57 |
10 |
Sí, asma |
No |
Bilateral |
Tubo de tórax, IOT, ECMO |
Falleció |
|
Xiang36 |
China |
1 |
M/67 |
10 |
Sí, enfisema |
Si |
Bilateral |
Tubo de tórax, IOT |
Falleció |
|
Ucpinar37 |
Turquía |
1 |
F/82 |
SD |
SD |
No |
Izquierdo |
Tubo de tórax |
Vivo |
|
Tucker et al.38 |
EE. UU. |
1 |
M/64 |
SD |
Sí, tabaquismo |
No |
Izquierdo |
IOT |
Falleció |
|
Gillespie39 |
EE. UU. |
1 |
M/70 |
SD |
No |
No |
Derecho |
IOT |
Falleció |
|
Vela40 |
España |
1 |
M/65 |
SD |
Sí, asma |
No |
Izquierdo |
SD |
SD |
|
* En años. EE. UU. = Estados Unidos; M = masculino; F = femenino; SD = sin datos; VM = ventilación mecánica; VMNI = ventilación mecánica no invasiva; IOT = intubación orotraqueal; BPAP = presión positiva de dos niveles en las vías respiratorias; ECMO = sistema de oxigenación por membrana extracorpórea. |
|||||||||


