Epidemiología descriptiva breve
La enfermedad por coronavirus 2019 (COVID-19) es una infección respiratoria causada por el virus del síndrome respiratorio agudo grave coronavirus 2 (SARS-CoV-2), identificado por primera vez en diciembre de 2019 en Wuhan, China. Desde entonces, se ha diseminado a todos los continentes y ha causado múltiples olas epidémicas. Hasta mayo de 2024, se han notificado más de 775 millones de casos confirmados y más de 7 millones de muertes a nivel mundial1. En México, hasta el 25 de junio de 2023 se han reportado más de 7.6 millones de casos acumulados y más de 334 mil muertes desde el inicio de la pandemia2, con una letalidad de 4.39%, comparada con la mundial de 0.9%. Esta diferencia en letalidad que muestra México en comparación con la mundial es probable que se deba a que el número de casos reportados en México subestima la verdadera carga de la enfermedad, debido a que solo una fracción de los casos se diagnostican y reportan. Aunque las cifras oficiales ofrecen una aproximación de la carga de enfermedad, se reconoce que existe una importante subestimación, debido a una baja proporción de casos diagnosticados por pruebas confirmatorias, especialmente durante las olas con mayor transmisión. La letalidad global reportada ha disminuido progresivamente desde el inicio de la pandemia, atribuible tanto a la inmunidad adquirida (por infección o vacunación) como a la disponibilidad de tratamientos más efectivos y sistemas de salud más adaptados3. La vigilancia epidemiológica internacional ha documentado que la distribución de casos, hospitalizaciones y muertes ha variado ampliamente entre regiones y países, influida por el acceso desigual a vacunas, servicios de salud, medidas de mitigación y presencia de comorbilidades en la población4.
Antes de que la Organización Mundial de la Salud (OMS) declarara el fin de la emergencia sanitaria mundial de la COVID-19 en mayo de 2023, la infección por SARS-CoV-2 provocó un exceso de muertes estimado en 15 millones solo en 2020 y 2021, y a medida que el SARS-CoV-2 se vuelve endémico, sigue siendo una causa importante de enfermedad en todo el mundo5.
Dinámica de la transmisión y excreción viral
La ruta principal de transmisión y propagación del SARS-CoV-2 es por vía aérea directa por contacto de persona a persona a una distancia corta (aproximadamente dos metros). El virus que se libera en las secreciones respiratorias cuando una persona infectada habla, tose, estornuda o canta, puede infectar a otra persona si se inhala o entra en contacto directo con las membranas mucosas. La infección también puede ocurrir si las manos de una persona están contaminadas por estas secreciones o al tocar superficies contaminadas y luego se tocan los ojos, la nariz o la boca, aunque es poco probable que las superficies contaminadas sean una vía importante de transmisión6. El SARS-CoV-2 también se ha identificado en muestras no respiratorias, incluidas heces, sangre, secreciones oculares y semen, pero el papel de estos sitios en la transmisión de acuerdo a la evidencia actual es poco probable7. Las gotitas respiratorias que se emiten cuando un individuo infectado habla, tose o estornuda tienen un tamaño relativamente grande de 5 a 10 μm, en contraste, los aerosoles son núcleos de gotitas respiratorias que se forman después de la evaporación y suelen tener un tamaño inferior a 5 µm8. Las gotitas respiratorias y los aerosoles expulsados durante un estornudo o la tos pueden viajar de 3.6 m hasta 7.9 m de distancia9; significativamente más lejos que la pauta de distanciamiento social de los 2 metros recomendada por los Centros para el Control y la Prevención de Enfermedades (CDC) de los Estados Unidos. Debido a su pequeño tamaño y, por lo tanto, a la influencia insignificante de la gravedad, los aerosoles generalmente permanecen a flote en el aire durante períodos de tiempo prolongados, lo que genera una amenaza adicional de transmisión aérea, especialmente en ambientes interiores con poca ventilación.
Las partículas virales que se encuentran en las gotitas respiratorias y aerosoles exhalados de los individuos infectados pueden unirse a las partículas PM2.5 de la atmósfera, sin embargo, es incierta la contribución de esta vía de transmisión al contexto de la pandemia10. La transmisión también ocurre a partir de intervenciones médicas como la toma de las muestras nasofaríngeas, intubación orotraqueal, ventilación invasiva y no invasiva, utilización de nebulizadores, cánula nasal de oxígeno de alto flujo, broncoscopia, etc.
Las tasas de transmisión más altas ocurren por contacto cercano y dentro de los hogares, pero en la mayoría de los casos (79%) se desconoce la fuente de exposición responsable de la transmisión11. La transmisión máxima ocurre entre 5 y 8 horas antes del inicio de síntomas, y es más alta en las primeras etapas del curso de la enfermedad, que es cuando los niveles de ARN viral en las muestras de vías respiratorias superiores son los más altos12. La transmisión después de 7 a 10 días de enfermedad es poco probable, en particular para pacientes inmunocompetentes con infección no grave. Un estudio de contactos demostró que aquellos que tuvieron exposición con pacientes infectados después de seis días posteriores al inicio de los síntomas no desarrollaron la infección13.
La duración del derramamiento viral es variable y puede incrementarse con la edad y la gravedad de la enfermedad. Los resultados de un metaanálisis, documentaron que la mediana de la detección del ARN viral en muestras respiratorias fue de 18 días a partir del inicio de los síntomas14 y en algunos individuos este se pudo detectar en el 5% de los casos en la quinta semana y hasta varios meses después15,16. Sin embargo, hay que aclarar que la identificación del RNA viral no necesariamente indica la presencia del virus viable17.
El virus con capacidad infecciosa solo se ha detectado en muestras respiratorias con altas concentraciones de ARN viral. Estas altas concentraciones de ARN viral se reflejan en un menor número de ciclos de amplificación de la reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR) necesarios para la detección. El umbral de ciclo (Ct) para la positividad del cultivo de muestras puede variar de 24 a 3218,19. Según los CDC de los Estados Unidos, tres días después de la recuperación clínica, si el ARN viral aún es detectable en las muestras de las vías respiratorias superiores, las concentraciones de ARN están generalmente por debajo de los niveles en los que el virus se puede aislar de forma fiable. Asimismo, es muy raro el aislamiento del virus infeccioso de las muestras de las vías respiratorias superiores a más de 10 días después del inicio de la enfermedad18,20.
Historia natural del virus SARS-CoV-2
El período de incubación, que es el tiempo entre la exposición al virus y la aparición de los síntomas de COVID-19, es de 5.2 días (IC 95%: 4.1-6.4). En algunos casos, puede ser tan corto como 36 horas o hasta 14 días. Los casos presintomáticos o asintomáticos también tienen la capacidad de transmitir la enfermedad. Los primeros transmiten la enfermedad pocos días antes del inicio de los síntomas, cuando la carga viral es más alta, sin ser conscientes de que están infectando a otros21. El riesgo de transmisión en casos presintomáticos es alto y, según algunos informes, contribuyó al 48% y 62% de las transmisiones en Singapur y China22. Aunque se reporta, ha sido difícil cuantificar el papel de los casos asintomáticos en la transmisión23. Es seguro suponer que en una proporción significativa de casos secundarios, la transmisión se produce antes del inicio de los síntomas y, en algunos casos, en ausencia de ellos.
R-nught (R0) es un concepto epidemiológico útil para el estudio de la transmisión de enfermedades, definido como el número promedio de casos nuevos generados por cada caso infectado. R0 es una medida de salud pública útil en términos de propagación de enfermedades y su eventual contención. No es un valor fijo y depende de una variedad de factores, como la susceptibilidad de la población a la infección, la demografía, la situación socioeconómica y la estacionalidad. Normalmente, el valor R0 varía entre menor de 1 si la enfermedad está controlada y mayor que 1 si se está propagando. A lo largo del curso de un brote de enfermedad, las intervenciones destinadas a controlar la propagación pueden describirse como intentos de reducir el valor de R024. El R0 promedio de COVID-19 se estima en 2.2 y 2.7 con un tiempo de duplicación de casos entre 6 a 7 días25. Dado que R0 es un valor medio, su significado puede quedar oculto por una distribución muy dispersa en la que un puñado de personas infectadas provocan la mayor parte de la transmisión secundaria. En el caso de la COVID-19, se estima que una pequeña fracción (10%) de los individuos infectados está causando el 80% de las infecciones secundarias26.
Comprender el riesgo de infección es importante para combatir el virus. El riesgo de transmisión del virus es variable según el escenario y depende tanto del tiempo de exposición como de la carga viral y el espacio físico. En un entorno cerrado con mala ventilación, grandes multitudes y contacto por tiempo prolongado con una persona infectada aumentan considerablemente la probabilidad de infección secundaria. En muchos casos, una sola persona infectada transmite el virus a un gran número de personas mientras asiste a eventos que reúnen a varias personas como conferencias, servicios religiosos, eventos deportivos o sociales. Cuanto más largo sea el período de exposición del grupo que permanece unido, la probabilidad de propagación viral es mayor. Los espacios interiores y mal ventilados son especialmente propicios para la transmisión. En un estudio de Japón, se estimó que las probabilidades de transmisión en un entorno cerrado eran 18.7 veces mayores en comparación con un entorno al aire libre27, de esta forma, la tasa de reproducibilidad (R0) del SARS-CoV-2 estimada en 328, se eleva a 11 en entornos cerrados como es el ambiente laboral29. La Asociación Médica de Texas desarrolló un cuadro de riesgo para COVID-19, basado en la exposición a diferentes escenarios en una escala del 1 al 10 y que se puede consultar en línea. A continuación, se exponen algunos ejemplos de los escenarios descritos en dicho cuadro con el riesgo asignado ordenados de menor a mayor: cargar gasolina 2, jugar tenis 2, comer en un restaurante al aire libre 4, ir a la playa 5, asistir en un centro comercial 5, nadar en una alberca pública 6, comer dentro de un restaurante 7, viajar en avión 7, trabajar en un gimnasio 8, asistir a un concierto o a un estadio 9, etc30.
Curso de la enfermedad
Una vez que la enfermedad se manifiesta, sigue una evolución en el tiempo que está determinada por dos mecanismos fisiopatogénicos distintos que se superponen; el primero desencadenado por el virus y el segundo por la respuesta inmune del hospedero. Siddiqi y Mehra proponen un sistema de clasificación de tres etapas con tres categorías de gravedad que se caracterizan por distintos hallazgos clínicos, respuesta al tratamiento y desenlace. La etapa I que ocurre durante los primeros días de la infección es en la que predomina la multiplicación de la carga viral, con síntomas como malestar general, fiebre y tos, entre otros, y se activa la respuesta inmune ante el virus (Figura 1)31. Los casos que se limitan a esta etapa se recuperan y el pronóstico es bueno. La etapa II se caracteriza por neumonía debida a la presencia del virus en el parénquima pulmonar con el desarrollo subsecuente de respuesta inflamatoria. La extensión de la neumonía y la intensidad de la respuesta inflamatoria tendrán repercusión en diferentes grados de hipoxia. A la etapa III llega una minoría de pacientes, es la etapa más grave de la enfermedad debido al desarrollo de un síndrome hiperinflamatorio y se manifiesta no sólo por hipoxia grave, sino también por manifestaciones extrapulmonares31.
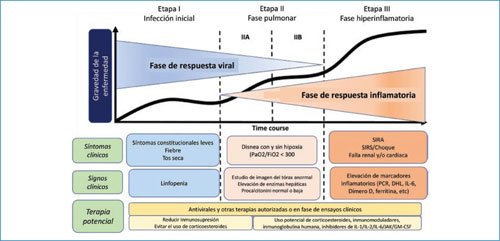
Figura 1. Clasificación de las etapas de la enfermedad COVID-19 y blancos terapéuticos potenciales. (tomada y adaptada de Siddiqi y Mehra.31). Con licencia de Elsevier número 5101931362917, del 04 de Julio de 2021.
El informe más amplio sobre casos de COVID-19, que reúne datos de 72.314 casos, demuestra que el 81% desarrolló enfermedad leve y que el 5% presentó una forma grave, caracterizada por insuficiencia respiratoria, choque séptico y disfunción multiorgánica, con una mortalidad del 50% en estos casos, principalmente en pacientes de más de 50 años. La tasa de letalidad general es del 2.3%, y en las personas de 60-69 años, de 70 a 79 años y en los mayores de 80 años, esta se incrementa al 3.6%, 8.0% y 14.8%, respectivamente32,33.
Las personas de todas las edades corren el riesgo de contraer la infección y la enfermedad grave. Sin embargo, los pacientes de edad ≥ 60 años y los pacientes con comorbilidades médicas subyacentes (diabetes, obesidad, enfermedad pulmonar crónica, enfermedad renal crónica, enfermedad cardiovascular, cáncer, pacientes con trasplante de órganos sólidos o células madre hematopoyéticas) tienen un mayor riesgo de desarrollar una infección grave por COVID-19. Los resultados de un análisis realizado por Stokes et al. de los casos confirmados reportados a los CDC durante el 22 de enero al 30 de mayo de 2020, mostraron que los pacientes con COVID-19 que requirieron hospitalización fue seis veces mayor en aquellos con condiciones médicas preexistentes que en aquellos sin condiciones médicas (45.4% versus 7.6%), asimismo, el riesgo de muerte fue 12 veces mayor en aquellos con condiciones médicas preexistentes que en aquéllos sin condiciones médicas (19.5% versus 1.6%)34. Los datos relativos a las diferencias de género en la COVID-19 sugieren que los hombres corren el riesgo de desarrollar una enfermedad grave y un aumento de la mortalidad debido a la COVID-19 en comparación con las mujeres35.
Los pacientes pueden presentar una serie de manifestaciones clínicas que van desde la ausencia de síntomas hasta la enfermedad crítica asociada a la insuficiencia respiratoria, el choque séptico y la falla orgánica múltiple. La gran mayoría de los pacientes sintomáticos suelen presentar una combinación variable de cualquiera de los siguientes síntomas: fiebre, tos y dificultad respiratoria, dolor de garganta, anosmia, disgeusia, anorexia, náuseas, malestar general, mialgias y diarrea. Stokes et al. informaron que entre 373,883 casos sintomáticos confirmados de COVID-19 en los Estados Unidos, el 70% de ellos experimentaron fiebre, tos y dificultad para respirar, el 36% informó de mialgias y el 34% cefalea34. La enfermedad COVID-19, además de los signos y síntomas descritos previamente, también produce manifestaciones extrapulmonares como cardíacas, neurológicas, hematológicas, renales, hepatobiliares, endocrinológicas y gastrointestinales. En este mismo contexto, un metaanálisis de 8,697 pacientes en China documentó las siguientes alteraciones en los estudios de laboratorio clínico como leucopenia (23.5%), linfopenia (47.6%), alteración de la función hepática (26.4%) y renal (10.9%), niveles elevados de proteína C reactiva (65,9%), enzimas cardíacas (49.4%) dímero D (20.4%) y procalcitonina (16.7%)36. Los hallazgos radiográficos comunes en estos pacientes incluyeron opacidades bilaterales multifocales en las radiografías de tórax y opacidades bilaterales periféricas en vidrio esmerilado, con o sin áreas de consolidación en la tomografía computada de tórax.
Con base en la gravedad de la enfermedad, los Institutos Nacionales de la Salud (NIH) han publicado unas directrices que clasifican la COVID-19 en cinco tipos distintos en los que se pueden agrupar los adultos con infección por SARS-CoV-2. Se tiene en cuenta la gravedad de los síntomas clínicos, las anomalías de laboratorio y radiográficas, la estabilidad hemodinámica y la función de los órganos:
-Infección asintomática o presintomática: Individuos con prueba positiva de SARS-CoV-2 sin ningún síntoma clínico consistente con COVID-19.
-Enfermedad leve: Individuos que presentan cualquier síntoma de COVID-19 como fiebre, tos, dolor de garganta, malestar general, dolor de cabeza, dolor muscular, náuseas, vómitos, diarrea, anosmia o disgeusia, pero sin dificultad respiratoria ni imágenes torácicas anormales.
-Enfermedad moderada: Individuos que presentan síntomas clínicos o evidencia radiológica de enfermedad del tracto respiratorio inferior y que tienen una saturación de oxígeno (SpO2) ≥ 94% al aire ambiente
-Enfermedad grave: Individuos que tienen una saturación de oxígeno (SpO2) ≤ 94% al aire ambiente; una relación entre la presión parcial de oxígeno arterial y la fracción de oxígeno inspirado, (PaO2/FiO2) < 300 con frecuencia respiratoria > 30 respiraciones/min u opacidades pulmonares > 50% en la radiografía de tórax o tomografía computada y neutrofilia37.
-Enfermedad crítica: Individuos que presentan insuficiencia respiratoria aguda, choque séptico y/o disfunción orgánica múltiple. Los pacientes con enfermedad grave pueden desarrollar el síndrome de dificultad respiratoria aguda (SDRA) que tiende a ocurrir aproximadamente una semana después del inicio de los síntomas.
Prevención
La prevención de la infección por SARS-CoV-2 ha evolucionado de forma sustancial desde el inicio de la pandemia de COVID-19, adaptándose a la disponibilidad de vacunas, a la evidencia científica emergente y a la dinámica de transmisión de nuevas variantes. En la actualidad, las estrategias preventivas incluyen intervenciones farmacológicas (vacunación) y no farmacológicas (uso de mascarillas, ventilación, higiene, pruebas diagnósticas, aislamiento y eliminación de la cuarentena).
La vacunación constituye la principal herramienta de prevención de COVID-19 a nivel individual y comunitario. Diversos estudios han demostrado que la inmunización reduce el riesgo de infección sintomática, hospitalización y muerte38,39. Si bien la eficacia contra la infección puede disminuir con la aparición de nuevas variantes, la protección frente a enfermedad grave y desenlaces fatales se mantiene de manera significativa40.
Los CDC y la OMS recomiendan la aplicación periódica de dosis de refuerzo, en especial en personas mayores de 60 años, pacientes inmunocomprometidos, embarazadas y personal de salud, priorizando formulaciones actualizadas contra variantes circulantes41,42.
De las medidas no farmacológicas, el uso de mascarillas fue una de las primeras intervenciones de control y continúa siendo una medida eficaz, particularmente en contextos de alta transmisión comunitaria y en espacios cerrados con poca ventilación. Las mascarillas de alta eficiencia (N95, KN95 o equivalentes) ofrecen mayor protección que las mascarillas quirúrgicas o de tela43.
Otra de las medidas no farmacológicas es la mejora de la ventilación en interiores, que disminuye la concentración de partículas virales en el aire, reduciendo el riesgo de transmisión. Se recomienda favorecer la ventilación natural mediante apertura de ventanas, así como el uso de sistemas de filtración (HEPA) en lugares cerrados con alta concurrencia44. Las medidas básicas de higiene, como cubrirse la boca y nariz al toser o estornudar y el lavado frecuente de manos con agua y jabón y el uso de solución hidroalcohólica, continúan siendo esenciales para limitar la propagación de SARS-CoV-2 y otros virus respiratorios45.
La disponibilidad de pruebas rápidas y moleculares ha facilitado la identificación temprana de casos. El monitoreo de síntomas y la realización de pruebas en personas con sospecha de exposición o síntomas compatibles permiten implementar aislamiento de manera oportuna, reduciendo el riesgo de transmisión46.
En marzo de 2024, los CDC actualizaron sus directrices sobre la duración del aislamiento en personas con infección confirmada por SARS-CoV-2. A diferencia de las recomendaciones iniciales, que establecían un periodo fijo de cinco días de aislamiento seguido del uso de mascarilla durante otros cinco días47,48, la nueva orientación se basa en la condición clínica del paciente. Actualmente, se indica que los pacientes sintomáticos deben permanecer en aislamiento hasta que se cumplan dos criterios: (1) haber transcurrido al menos 24 horas sin fiebre en ausencia de antipiréticos y (2) mejoría general de los síntomas49. Una vez alcanzados estos criterios, el aislamiento domiciliario puede darse por concluido, independientemente del número total de días desde el inicio de los síntomas. Los CDC recomiendan mantener precauciones adicionales durante los cinco días posteriores, tales como el uso de mascarilla de alta eficiencia, evitar el contacto con personas vulnerables, asegurar buena ventilación y reforzar la higiene.
La cuarentena, entendida como la restricción de actividades en personas asintomáticas con exposición a un caso confirmado, fue ampliamente utilizada durante 2020 y 2021, con períodos recomendados de hasta 14 días, reducidos posteriormente a siete días con prueba negativa. En agosto de 2022, los CDC eliminaron la recomendación de cuarentena para contactos, sustituyéndola por la indicación de vigilar síntomas durante 10 días, usar mascarilla y realizar una prueba alrededor del día cinco tras la exposición. Finalmente, con la actualización de marzo de 2024, los CDC confirmaron que la cuarentena ya no es necesaria. La estrategia actual consiste en la observación clínica activa y medidas de protección, con aislamiento únicamente en caso de presentar síntomas o un resultado positivo50,51.
En resumen, las medidas preventivas frente al SARS-CoV-2 han transitado de modelos rígidos a enfoques dinámicos y adaptados a la evolución epidemiológica. La vacunación sigue siendo el pilar fundamental, complementada con intervenciones no farmacológicas como el uso de mascarilla en contextos de riesgo, la ventilación de espacios y la higiene. El aislamiento continúa siendo necesario en casos confirmados, pero se aplica con base en criterios clínicos más que en periodos fijos de tiempo, mientras que la cuarentena ha dejado de recomendarse en personas expuestas asintomáticas.
Proyección futura de la pandemia
Aunque la fase de emergencia internacional de la COVID-19 fue declarada como finalizada por la OMS en mayo de 2023, el SARS-CoV-2 continúa circulando globalmente como un patógeno respiratorio relevante. En el futuro previsible, se espera que la COVID-19 transite a una forma endémica, con circulación estacional y picos esporádicos asociados a nuevas variantes o disminución de la inmunidad poblacional52.
Las vacunas y tratamientos antivirales han contribuido significativamente a reducir la severidad de la enfermedad, hospitalizaciones y muertes. Sin embargo, la prevención seguirá dependiendo parcialmente de intervenciones no farmacológicas, sobre todo en grupos vulnerables y durante picos de transmisión. La posibilidad de eliminar el virus parece inviable en el corto plazo, debido a la alta transmisibilidad del SARS-CoV-2, la inmunidad incompleta y transitoria, así como la aparición continua de variantes con escape inmunológico parcial53.
Desde su aparición, el virus ha generado múltiples variantes, algunas de las cuales han sido clasificadas como variantes de preocupación (VOC) por su mayor transmisibilidad o evasión inmune. Hasta la fecha, las principales VOC identificadas han sido Alpha, Beta, Gamma, Delta y Ómicron, siendo esta última la de mayor circulación desde finales de 2021. Dentro de la familia Ómicron, subvariantes como XBB.1.5 y JN.1 han dominado en distintos momentos desde 2023, presentando mayor transmisibilidad, pero menor letalidad comparada con variantes anteriores.
Aunque las vacunas actuales ofrecen buena protección contra enfermedad grave y muerte, su efectividad contra la infección disminuye con el tiempo y ante nuevas variantes. La inmunidad de rebaño completa no se ha alcanzado ni es esperable a mediano plazo, debido a factores como la heterogeneidad en cobertura vacunal, la evolución viral y la inmunidad parcial inducida por infecciones previas53.
Las proyecciones a cinco años sugieren que la incidencia de COVID-19 dependerá del grado de inmunidad en la población, la duración de la inmunidad postinfección o vacunación y la dinámica de aparición de nuevas variantes. También influirán la estacionalidad, la inmunidad cruzada con otros coronavirus y las políticas sanitarias locales53,54. La vigilancia genómica y la adaptación continua de vacunas serán herramientas clave para el control sostenido de la enfermedad.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
