Introducción
El 31 de diciembre de 2019, las autoridades de salud de China informaron sobre la presencia de 27 casos de síndrome respiratorio agudo de etiología desconocida en Wuhan. Posteriormente, se identificó un nuevo coronavirus, el SARS-CoV-2, como su posible causa. Esta enfermedad se extendió por todo el mundo. En México, el primer caso confirmado se reportó el 27 de febrero de 2020, y el 11 de marzo la Organización Mundial de la Salud emitió la declaración de pandemia de COVID-19.
Desde el inicio de la pandemia se describieron tres etapas clínicas de gravedad de la enfermedad. La etapa inicial se caracteriza por la infección por SARS-CoV-2; se pueden desarrollar síntomas como rinorrea, cefalea y malestar general, similares a los de un catarro común. La segunda etapa se caracteriza por inflamación pulmonar y coagulopatía, que pueden desarrollarse de forma consecutiva o superpuesta, con elevación de biomarcadores inflamatorios como la proteína C reactiva, la ferritina, las interleucinas 6 y 1, y el dímero D, los cuales se asocian con desarrollo de síndrome de insuficiencia respiratoria aguda (SIRA) y peor pronóstico. Finalmente, la tercera etapa de la enfermedad se caracteriza por fibrosis. Todas estas etapas se manifiestan con escenarios clínicos diversos, desde una forma asintomática hasta una forma grave caracterizada por SIRA con disfunción orgánica múltiple. La mortalidad de la COVID-19 durante la pandemia fue del 5.4%; sin embargo, la comorbilidad, incluyendo diabetes mellitus e hipertensión arterial, y la edad avanzada, la elevan considerablemente1,2.
Se han publicado numerosos artículos con datos epidemiológicos, características clínicas y posibles tratamientos para la COVID-19, pero los informes patológicos han sido menos frecuentes, limitando así el conocimiento global y el desenlace de la infección3. Una limitante para estos estudios fue el riesgo que conllevaba la toma de tejido, por lo que la bioseguridad desempeñó un papel importante. El Royal College of Pathologists publicó una guía de bioseguridad para estudios post mortem en sujetos con infección por SARS-CoV-2, con la finalidad de reducir el riesgo de trasmisión del virus4.
Hallazgos histopatológicos
Las series de casos con hallazgos histopatológicos se centraron principalmente en la descripción de lesiones pulmonares en distintas fases, la formación de membrana hialina e hiperplasia típica de neumocitos, y la presencia de trombos y fibrina en los vasos arteriales pequeños, compatibles con coagulopatía5. Se han registrado al menos tres patrones histológicos primarios de lesión pulmonar: 1) patrón epitelial, caracterizado por daño alveolar difuso (DAD) con diversos grados de organización, denudación e hiperplasia de neumocitos, así como posibles cambios citopáticos; 2) patrón vascular, caracterizado por fibrina intraalveolar difusa o presencia de trombos microvasculares (fibrina); y 3) patrón fibrótico, que incluye DAD fibrótico o fibrosis intersticial.
De acuerdo con Katzenstein y Askin6, el DAD es una reacción inespecífica del pulmón ante una multitud de agentes agresores. El denominador común es la lesión endotelial y alveolar que determina una exudación de fluidos y células, que en ocasiones progresa a fibrosis intersticial pulmonar extensa. El hallazgo patológico más característico de la etapa aguda del DAD es la presencia de membranas hialinas que al microscopio óptico se visualizan como un material homogéneo, eosinófilo y que se extiende sobre la superficie interna de los alvéolos. Las membranas hialinas están conformadas por restos necróticos de células epiteliales y proteínas séricas que han pasado desde el torrente circulatorio al espacio alveolar debido al aumento en la permeabilidad de la barrera alveolocapilar. La apariencia del DAD depende del tiempo transcurrido entre la exposición al factor de riesgo y el estudio histológico. Esquemáticamente, se pueden reconocer tres fases consecutivas: una precoz o exudativa, caracterizada por exudado intraalveolar, membranas hialinas e infiltrado celular principalmente de linfocitos, células plasmáticas y macrófagos; una intermedia o proliferativa, caracterizada por hiperplasia, atipia y mitosis de neumocitos tipo II con trombosis de pequeñas arterias pulmonares; y una fase final de fibrosis u organización, caracterizada por engrosamiento de la membrana alveolocapilar, proliferación de fibroblastos (en particular en el intersticio) y fibrosis. En los casos más graves, la fibrosis puede progresar en semanas reestructurando todo el parénquima pulmonar y formando una imagen pulmonar en panal de abeja con sustitución prácticamente total del espacio alveolar. Es importante destacar que las distintas fases se pueden superponer, por lo que es posible encontrar en un mismo paciente varias fases evolutivas7.
La revisión sistemática realizada por Polak et al.7 reveló que algunos hallazgos histopatológicos en los pulmones difieren significativamente entre la COVID-19 y el SIRA convencional y otras formas de neumonitis viral. Los cambios pulmonares que se encuentran típicamente en el SIRA incluyen neumonía intersticial aguda con edema y DAD con diversos grados de organización8. Los hallazgos histopatológicos en la neumonitis por influenza a menudo incluyen trombosis capilar y de vasos pequeños, edema intersticial, infiltrados inflamatorios intersticiales neutrófilos y linfoplasma histiocíticos, formación de membranas hialinas, grados variables de edema o hemorragia intraalveolar y DAD agudo, además de bronquitis necrotizante y bronquiolitis. Las etapas posteriores de la enfermedad incluyen DAD organizado, fibrosis, regeneración epitelial y metaplasia escamosa7. En otras infecciones por coronavirus, como el síndrome respiratorio de Oriente Medio y el síndrome respiratorio agudo grave previo causado por el SARS-CoV, los pacientes desarrollan una oclusión de las vías respiratorias pequeñas por detritos debido a la denudación de las vías respiratorias, así como infiltrados de células inflamatorias, hemorragia, edema alveolar y formación de membranas hialinas, características clínicas típicas de la etapa exudativa del DAD9. En contraste, el cuadro histopatológico de la neumonitis relacionada con COVID-19 parece abarcar patrones epiteliales, vasculares y fibróticos de lesión pulmonar10.
Al analizar los patrones histopatológicos de pacientes en diferentes etapas de la enfermedad en relación con el inicio de los síntomas, algunos estudios sugieren una línea de tiempo relativamente clara. Los cambios epiteliales, incluidos DAD, denudación y atipia reactiva de neumocitos, estuvieron casi siempre presentes en todas las etapas de la enfermedad; además, los cambios vasculares, incluyendo daño microvascular, trombos, depósitos de fibrina intraalveolar y otras características de la neumonía fibrinosa y organizada aguda, también ocurrieron durante las primeras fases de la infección sintomática por SARS-CoV-210. Este patrón vascular de la lesión pulmonar por COVID-19 ha sido predominante, en comparación con el SIRA convencional y la influenza, y está en consonancia con los estudios clínicos que informan de un impresionante 49% de casos de episodios trombóticos. Esto concuerda con la presencia del receptor de la enzima convertidora de la angiotensina 2 (ACE2) tanto en el epitelio alveolar como en el endotelio capilar. Por otro lado, los cambios de fibrosis intersticial generalmente aparecieron después de varias semanas del inicio de los síntomas, aunque algunos pacientes presentaron fibrosis en una etapa temprana. Este hallazgo probablemente se debió a una enfermedad pulmonar preexistente y no a la infección por SARS-CoV-2.
Otros estudios han investigado la correlación entre los parámetros ventilatorios, los hallazgos tomográficos y los patrones histológicos identificados. La tomografía computada de tórax se ha descrito con imágenes típicas de múltiples opacidades bilaterales en vidrio deslustrado o consolidación. En los estudios de laboratorio, la cuenta de leucocitos era normal en la mayoría de los pacientes, mientras que la linfocitopenia fue frecuente y los biomarcadores de inflamación, como la proteína C reactiva, el dímero D y la creatina cinasa, estuvieron elevados en la mayoría de los casos11. Estos resultados han permitido conocer el comportamiento del virus en varios sistemas.
Al ser una enfermedad emergente, la fisiopatología no es conocida por completo. Se cree que los estudios post mortem pueden ayudar a comprenderla y direccionar o modificar el manejo terapéutico establecido hasta hoy. La literatura acerca de los cambios histopatológicos en pacientes infectados por SARS-CoV-2 es limitada, por lo que planteamos analizar, describir y correlacionar los hallazgos histopatológicos con la evolución clínica, bioquímica y radiológica de los pacientes fallecidos durante la pandemia de COVID-19 en el Instituto Nacional de Enfermedades Respiratorias Ismael Cosío Villegas (INER).
La experiencia del INER
Se cuenta con hallazgos histopatológicos post mortem de 40 pacientes (28 hombres y 12 mujeres), con una edad media de 55.4 años (desviación estándar: 12.6). Con respecto a la comorbilidad, 8 pacientes (20%) tenían hipertensión, 1 (2.5%) cardiopatía isquémica, 1 (2.5%) enfermedad renal crónica en tratamiento con hemodiálisis, 25 (62.5%) distintos grados de obesidad, 15 (37.5%) antecedente de alcoholismo crónico y 8 (20%) enfermedad pulmonar obstructiva crónica (EPOC). Todos los pacientes presentaron síntomas; el inicio de los síntomas antes de su ingreso tuvo una duración promedio de 8.5 días (intervalo de confianza [IC]: 6.75-15), y la estancia hospitalaria fue en promedio de 11 días (IC: 6.75-15.25). En el momento de la hospitalización, todos los pacientes tenían características clínicas (disnea, tos, mialgias, fatiga, cefalea, fiebre, anosmia, disgeusia y diarrea) y radiológicas de neumonía intersticial, clasificándose según su patrón tomográfico en tres etapas de acuerdo con la progresión. En el momento del ingreso hospitalario, la saturación de oxigeno resultó en promedio del 82% (desviación estándar: 12.5), con un índice de oxigenación (PaO2/FiO2) de 130 (IC: 97-164). En 39 pacientes se requirió ventilación mecánica, con una mediana de 11.5 días (IC: 8.25-17). Durante la estancia hospitalaria se observó daño renal agudo no identificado al ingreso en 27 pacientes (67.5%). En 19 pacientes (47.5%) se identificó desarrollo de infección secundaria por Pseudomonas (5), Acinetobacter (5), Klebsiella (3), Staphylococcus (3) y Candida (3). Con respecto al tratamiento, 17 pacientes recibieron ritonavir y oseltamivir, 23 (57.5%) recibieron antibióticos de distintos tipos, en 21 (52.2%) se administró hidroxicloroquina, y en 5 (12.5%) tocilizumab. En 25 pacientes (62.5%) se utilizó metilprednisolona y 34 (85%) requirieron vasopresores durante su estancia hospitalaria.
En la tabla 1 y la figura 1 se resumen los seis patrones histológicos identificados en el examen microscópico de los pulmones. En todas las muestras analizadas se tomó en cuenta el patrón predominante de cada pieza, aunque en la mayoría de los casos se encontró una combinación de distintos patrones (Fig. 2). Los patrones más frecuentes fueron daño alveolar agudo (n = 23), infiltrado celular crónico (n = 10) y patrón de cambios mínimos (n = 7). El patrón de fibrosis se encontró en 38 pacientes, con afectación < 20%; el patrón de llenado alveolar fue descrito en todos los pacientes, en < 30% de la pieza; y el patrón nodular estuvo presente en 7 pacientes, en < 10% de la pieza. En la tabla 2 se muestran los parámetros clínicos de acuerdo con el patrón histológico de lesión pulmonar más frecuente.
Tabla 1. Patrones histopatológicos pulmonares hallados en COVID-19 grave
| Patrón histológico | Elementos en el patrón |
|---|---|
| 1. Daño alveolar difuso | Exudado agudo en el interior de los alveolos con llenado parcial, formación de membranas hialinas, depósitos de tejido de granulación y proliferación de fibroblastos |
| 2. Fibrosis | Sustitución del intersticio por tejido fibroso que es una acumulación en exceso de componentes de la matriz extracelular, principalmente colágeno |
| 3. Infiltrado celular crónico | Ensanchamiento intersticial a expensas de proliferación principalmente de linfocitos y células plasmáticas |
| 4. Llenado alveolar | Llenado u ocupación de la totalidad del espacio alveolar por elementos celulares, como macrófagos, linfocitos y neutrófilos, y no celulares, como fibrina y detritos |
| 5. Nodular | Uno o varios nódulos de diversos tamaños y formas; se distingue una interfase entre la lesión nodular y el pulmón normal |
| 6. Cambios mínimos | La arquitectura alveolar se encuentra notablemente preservada en el estudio microscópico panorámico (4×), pero la observación estructural detallada (40×) demuestra daño multifocal en las paredes alveolares, el intersticio, la vía aérea pequeña y los vasos sanguíneos |
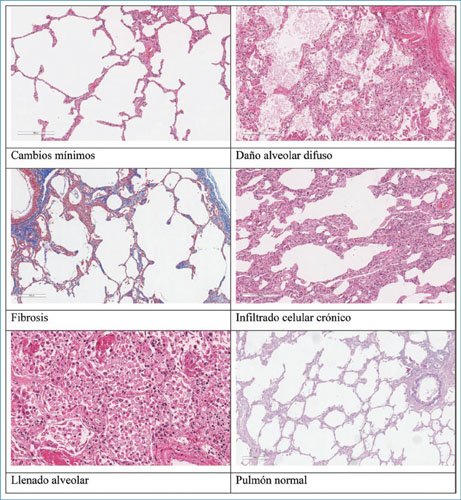
Figura 1. Imágenes ilustrativas de los patrones morfológicos pulmonares de los pacientes con COVID-19 grave.
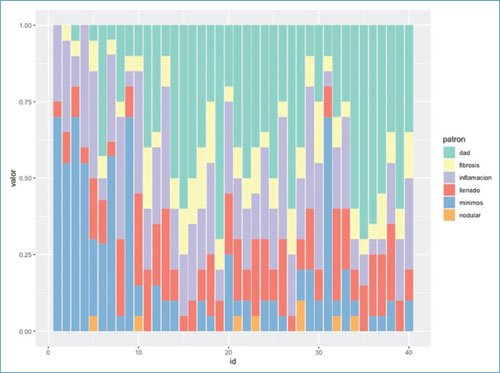
Figura 2. Ilustración gráfica de la distribución de los patrones histopatológicos pulmonares de 40 pacientes fallecidos por COVID-19 grave.
Tabla 2. Características clínicas de los pacientes según el patrón histológico de lesión pulmonar
| Características | Todos (n = 40) | Patrón histológico | p | ||
|---|---|---|---|---|---|
| Lesión pulmonar aguda (n = 23) | Infiltrado inflamatorio crónico (n = 10) | Cambios mínimos (n = 7) | |||
| Edad, años | 55.4 (12.6) | 55.2 (11.7) | 59.4 (14.7) | 50.4 (3.2) | 0.50 |
| Sexo, H/M, n (%) | 28/12 (70/30) | 17/6 (74/.26) | 6/4 (60/40) | 5/2 (71/29) | 0.80 |
| Comorbilidad | |||||
| Diabetes | 14 (35) | 8 (57.14) | 4 (28.6) | 2 (14.3) | 1 |
| Hipertensión | 8 (20) | 11 (68.75) | 3 (18.8) | 2 (12.5) | 0.50 |
| Cardiovascular | 1 (2.5) | ||||
| EPOC | 8 (20) | 4 (50) | 1(12.5) | 3 (37.5) | 0.30 |
| Enfermedad renal crónica | 1 (2.5) | 0 | 1 (100) | 0 | 0.43 |
| Obesidad | 25 (62.5) | 16 (64.4) | 5 (20) | 4 (16) | 0.60 |
| Alcoholismo | 15 (37.5) | 8 (53.3) | 4 (26.6) | 3 (20) | 1 |
| Síntomas | |||||
| Tos | 26 (65) | 13 (50) | 6 (23.1) | 7 (26.9) | 0.09 |
| Mialgia o fatiga | 25 (62.5) | 14 (56) | 7 (28) | 4 (16) | 0.80 |
| Cefalea | 13 (32.5) | 6 (46.15) | 4 (30.8) | 3 (23.1) | 0.59 |
| Diarrea | 4 (10) | 2 (50) | 0 | 2 (50) | 0.18 |
| Disnea | 36 (90) | 20 (55.6) | 9 (25) | 7 (19.4) | 1 |
| Fiebre | 37 (92.5) | 21 (56.8) | 9 (24.3) | 7 (18.9) | 1 |
| Anosmia | 5 (12.5) | 3 (60) | 2 (40) | 0 | 0.68 |
| Disgeusia | 10 (25) | 7 (70) | 2 (20) | 1 (10) | 0.69 |
| SpO2 | 82.5 (12.6) | 84.57 (11.8) | 75.8 (14.2) | 85.14(10.8) | 0.15 |
| PaO2/FiO2 | 130 (97-165) | 129 (98-148) | 150 (100-162) | 130 (82-176) | 0.63 |
EPOC: enfermedad pulmonar obstructiva crónica; FiO2: fracción inspirada de oxígeno; H: hombre; M: mujer; PaO2: presión de oxígeno arterial; SpO2: saturación de oxígeno.
Los datos se muestran en frecuencias y porcentaje entre paréntesis; para la SpO2 se indican el valor promedio y el valor intercuartil entre paréntesis.
Con respecto a la correlación con los patrones histológicos predominantes, ningún dato resultó estadísticamente significativo; no obstante, destaca el predominio del patrón de DAD como el más frecuente en todas las muestras tomadas en los pacientes con más comorbilidad. Este grupo registró un mayor número de síntomas a su ingreso hospitalario y una menor saturación de oxígeno en el grupo de infiltrado inflamatorio crónico, sin manifestar una diferencia significativa entre los tres grupos (tabla 2). En el análisis de la información no se encontró ninguna diferencia estadística entre los tres grupos predominantes. El grupo que requirió más tiempo de ventilación mecánica fue el de patrón DAD, que desarrolló daño renal e infecciones secundarias con más frecuencia; sin embargo, no hubo diferencias significativas con respecto a las intervenciones farmacológicas de tratamiento específico. En la figura 3 se ilustran las curvas de sobrevida durante la hospitalización por grupos de pacientes de acuerdo con el patrón histológico; no se observa una diferencia estadísticamente significativa. Existe una combinación de seis patrones histológicos característicos en todas las piezas con predominio del patrón de daño alveolar agudo, el cual aumentaba en porcentaje de presencia en la pieza con respecto al avance de la pandemia y la temporalidad de la toma de las biopsias, con una posibilidad de relación con respecto al avance de los meses de la pandemia y el uso de múltiples tratamientos.
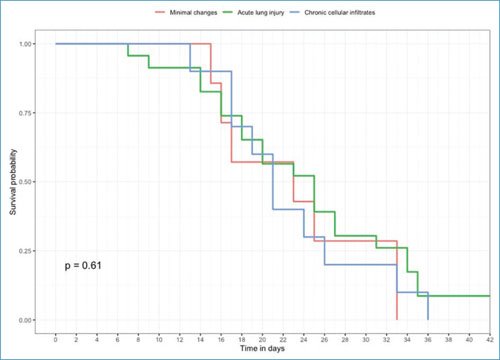
Figura 3. Curva de sobrevida (Kaplan-Meier) de los pacientes graves fallecidos por COVID-19, de acuerdo con el patrón histológico.
Los hallazgos histopatológicos en la neumonitis por influenza a menudo incluyen trombosis capilar y de vasos pequeños, edema intersticial, infiltrados inflamatorios intersticiales neutrófilos y linfoplasmocíticos, formación de membranas hialinas, grados variables de edema o hemorragia intraalveolar, y DAD agudo, además de bronquitis necrotizante y bronquiolitis (Fig. 4). Las etapas posteriores de la enfermedad incluyen DAD organizado, fibrosis, regeneración epitelial y metaplasia escamosa. En otras infecciones por coronavirus, como el síndrome respiratorio de Oriente Medio y el síndrome respiratorio agudo severo previo causado por el SARS-CoV, los pacientes desarrollan una pequeña oclusión de las vías respiratorias debido a la denudación de las vías respiratorias, así como infiltrados de células inflamatorias, hemorragia, edema alveolar y formación de membranas hialinas, características clínicas típicas de la etapa exudativa del DAD. En nuestros hallazgos, la denudación de las vías respiratorias no ha sido un hallazgo característico. El daño vascular de la lesión pulmonar por COVID-19 fue identificado con frecuencia en las muestras tomadas, en comparación con el SIRA convencional y la influenza. En numerosos estudios, este daño vascular ha sido relacionado con la presencia del receptor ACE2 tanto en el epitelio alveolar como en el endotelio capilar. Los cambios fibróticos se han descrito después de 3 semanas del inicio de los síntomas; aunque en nuestro estudio la fibrosis estuvo presente en 38 pacientes desde el inicio de la pandemia, no fue un patrón predominante. Se ha propuesto que este hallazgo puede estar relacionado con la preexistencia de EPOC.
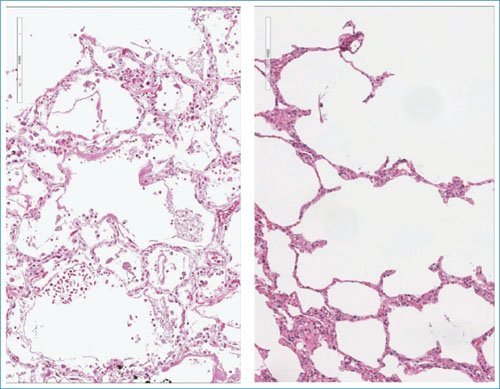
Figura 4. Comparación de los hallazgos histológicos en la influenza H1N1 y la COVID-19. El panel de la izquierda corresponde a una fotomicrografía de tejido pulmonar afectado por influenza H1 N1, que muestra daño alveolar difuso con formación de membranas hialinas y tejido de granulación intraalveolar; no hay notable daño intersticial ni microvascular (HyE, 20×). El panel derecho es una fotomicrografía que muestra tejido pulmonar afectado por COVID-19, con daño en las paredes alveolares caracterizado por neumonitis y obstrucción microvascular a expensas de microtrombos fibrinosos (HyE, 20×).
Consideraciones finales
La conexión entre los hallazgos patológicos y el curso clínico de la COVID-19 indica la posibilidad de que la patogenia siga un patrón secuencial. En la fase inicial de la infección viral, las células epiteliales respiratorias se infectan y, por tanto, predominan los cambios epiteliales con evidencia de actividad viral. El aclaramiento viral subsiguiente disminuye en los pacientes con enfermedad grave o con factores de riesgo subyacentes. La presencia de lesión pulmonar epitelial con hiperplasia y atipia de neumocitos y multinucleación, posiblemente representando efectos citopáticos virales, incluso en estadios posteriores de COVID-19, apoya este hallazgo. A partir de nuestros resultados en la población analizada en el INER, consideramos que la COVID-19 presenta etapas de forma consecutiva o simultánea.
Financiamiento
Los autores declaran que no hubo financiamiento.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.