Introducción
Las variantes anatómicas del árbol traqueobronquial son poco comunes, se presentan en el 1 a 12% de la población en general1. El isomerismo bronquial se refiere a un trastorno de la lateralidad broncopulmonar; el isomerismo bronquial izquierdo se caracteriza por pulmones bilobulados bilaterales, mientras que el isomerismo bronquial derecho se caracteriza por pulmones trilobulados bilaterales2. El isomerismo bronquial suele ser asintomático, sin embargo, pueden manifestarse como episodios recurrentes de tos, hemoptisis o infección3,4.
Los trastornos de la lateralidad pulmonar se han asociado a riesgo elevado de cáncer. En la literatura se han reportado casos de situs inversus pulmonar asociado a cáncer gástrico, rectal y pancreático5.
El tejido pulmonar contiene células neuroendocrinas localizadas en el epitelio bronquial, las cuales pueden presentar hiperplasia como parte de una respuesta inflamatoria crónica. Cuando la hiperplasia difusa idiopática de células neuroendocrinas se extiende más allá de la membrana basal del epitelio bronquial adquiere el término de «tumorlet». El término tumorlet se puede traducir como un tumor de pequeño tamaño y, por lo tanto, es un término descriptivo, no histológico6. Hace referencia a una proliferación de células neuroendocrinas menor a 0.5 cm. Son tumores de comportamiento benigno cuyo diagnóstico suele ser incidental, constituyendo un hallazgo patológico sin significado clínico. Se ha descrito su asociación con diversas neoplasias, como cáncer de mama, pulmón y linfomas torácicos.
Presentamos el caso de una paciente que cursó con infecciones de repetición, las cuales condicionaron bronquiectasias de lóbulo inferior izquierdo, asociadas a variante anatómica de isomerismo bronquial derecho. En el resultado del análisis de patología del tejido resecado se obtuvo la presencia de tumorlet.
Presentación del caso
Mujer de 44 años con antecedente de bronquiectasias y múltiples neumonías de repetición. En el seguimiento presenta sobreinfección de bronquiectasias por Pseudomonas aeruginosa resistente. Se realiza imagen de tomografía (Fig. 1A) con alteración a nivel de la ramificación bronquial que sugiere sospecha de lóbulo pulmonar accesorio. Sin embargo, en la imagen de reconstrucción bronquial se evidencia presencia de tres lóbulos pulmonares izquierdos (Fig. 1B) con bronquio inferior acompañado de arteria lobar (Fig. 1C). Las pruebas de función pulmonar reportaron volumen espiratorio forzado en un segundo (FEV1) 0.9, capacidad vital forzada (FVC) 2.14, FEV1/FVC 42, capacidad de difusión del monóxido de carbono 18.1 ml/min/mmHg.
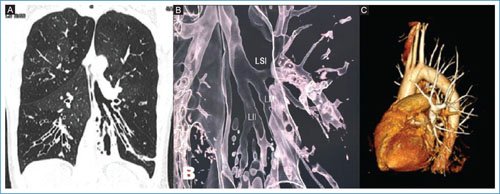
Figura 1. A: tomografía de tórax con ventana pulmonar y corte coronal a nivel de bronquio principal izquierdo. Se observan bronquiectasias arrosariadas (estrella) y división de tres bronquios: superior, medio e inferior. B: reconstrucción en tercera dimensión que demuestra carina secundaria con división de tres bronquios lobares. C: reconstrucción vascular del patrón arterial observando irrigación para lóbulo superior, medio e inferior de lado izquierdo.
Debido a la función pulmonar limítrofe, se programó para segmentectomía de lóbulo inferior izquierdo. En cirugía se evidenció pulmón izquierdo con presencia de tres lóbulos; superior, medio e inferior (Fig. 2A). Se realizó lobectomía inferior izquierda con manejo vascular y bronquial individual a nivel hiliar (Fig. 2B). Se colocó un drenaje pleural acanalado 24 Fr.
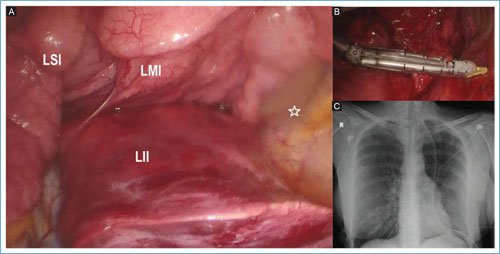
Figura 2. A: foto quirúrgica que demuestra cisura mayor y menor dividiendo pulmón izquierdo en lóbulo superior izquierdo (LSI), lóbulo medio izquierdo (LMI) y lóbulo inferior izquierdo (LII). La estrella marca la pared posterior del hemitórax izquierdo. B: manejo vascular de la arteria de lóbulo inferior izquierdo. C: radiografía de tórax en proyección posteroanterior del posquirúrgico inmediato con adecuada expansión pulmonar.
La paciente evolucionó favorablemente con retiro del drenaje pleural a los tres días del posquirúrgico (Fig. 2C) y egreso hospitalario a los cinco días.
El estudio de anatomía patológica reportó: bronquiectasias crónicas, tumorlet de 3 mm con grupos de células con patrón en crecimiento de nidos, citoplasma moderado con núcleos con cromatina en sal y pimienta. La inmunohistoquímica fue positiva a sinaptofisina y cromogranina.
Debido al aislamiento de Pseudomonas nuestra paciente cumplió esquema antibiótico con ceftazidima 14 días, posteriormente continuo con amikacina 14 días de forma ambulatoria.
Discusión
El árbol traqueobronquial es un sistema ramificado que transporta aire desde la tráquea a los ácinos. Existen diversas variaciones anatómicas; entre ellas, bronquios traqueales y cardiacos accesorios, divertículos traqueales, bronquios puente e isomerismo traqueobronquial. Si bien son una entidad poco frecuente, suelen ser de naturaleza asintomática. En los pacientes sintomáticos puede existir presencia de tos, hemoptisis y episodios recurrentes de infecciones respiratorias1.
El isomerismo bronquial es un trastorno de lateralidad pulmonar, se relaciona con una mutación en el gen ZIC3, gen regulador de la transcripción de dedo de zinc que determina la simetría izquierda y derecha del pulmón en el embrión humano.
El isomerismo bronquial fue descrito por primera vez por Bush en 1999. El isomerismo bronquial izquierdo se caracteriza por pulmones bilobulados bilaterales, mientras que isomerismo bronquial derecho se caracteriza por pulmones trilobulados bilaterales. Los síntomas suelen estar asociados a las anomalías asociadas. En el caso presentado, el lóbulo isomérico inferior izquierdo mostró alteraciones en la morfología bronquial caracterizadas por bronquiectasias, las cuales condicionaron eventos de infecciones de repetición con aislamiento de microorganismo resistente a la terapia antimicrobiana, situación que dictó conducta quirúrgica en nuestra paciente.
El tejido pulmonar contiene células neuroendocrinas localizadas en el epitelio bronquial y bronquiolar. La hiperplasia difusa idiopática de células neuroendocrinas (HDICN) es una entidad rara asociada a bronquitis oclusiva, fue reportada por primera vez por Aguayo en 1992. La HDICN se puede observar como parte de una reacción inflamatoria, la cual tiende a limitarse a la membrana basal epitelial bronquial. En pacientes con tumores carcinoides, la HDICN se ha considerado una lesión preneoplásica. El 47.4% de los pacientes con HDICN tienen carcinoides típicos, mientras que el 15.8% pueden tener carcinoides atípicos. Cuando la hiperplasia difusa de células neuroendocrinas involucra la membrana basal con una extensión menor a 5 mm se denomina «tumorlet», mientras que un tamaño mayor a 5 mm recibe el nombre de «carcinoide»7,8. En el aspecto histológico, los tumorlets tienen capacidad de captar o reducir las sales de plata, por lo que presentan positividad para tinciones argilófilas. En la inmunohistoquímica marcan para sinaptofisina y cromogranina. Poseen núcleo regular, redondo, ovalado o en forma de uso con cromatina finamente dispersa.
En tomografía computarizada (TC) de alta resolución, la hiperplasia difusa idiopática de células neuroendocrinas se caracteriza por perfusión en mosaico, debido al atrapamiento de aire, engrosamiento de la pared bronquial y bronquiectasias. El engrosamiento nodular de la pared bronquial es la correlación radiopatológica más directa de la proliferación de células neuroendocrinas submucosas9.
La sobrevida a 5 años para la hiperplasia difusa idiopática de células neuroendocrinas es del 83%, mientras que la sobrevida a 5 años de los tumores carcinoides típicos es del 93% y de los atípicos del 69%. De acuerdo con la última clasificación de la Organización Mundial de la Salud (OMS), la HDICN es una lesión preinvasiva, seguida de tumorlets y de los tumores carcinoides, por lo que en el contexto del seguimiento la European Society for Medical Oncology (ESMO) recomienda el seguimiento de por vida debido a que las recurrencias de los tumores carcinoides son frecuentes10.
Conclusiones
En este artículo presentamos el caso de una paciente de sexo femenino con cuadro infeccioso de bronquiectasias asociado a anomalía de la lateralidad pulmonar. El resultado de anatomía patológica reportó tumorlet de forma incidental. Si bien en la literatura existen solo reportes de caso, se trata de una entidad de sospecha ante pacientes con variantes en la morfología del árbol traqueobronquial y el riesgo de neoplasias en esta población.
Financiamiento
La realización del presente trabajo no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han seguido los protocolos de confidencialidad de su institución, han obtenido el consentimiento informado de los pacientes, y cuentan con la aprobación del Comité de Ética. Se han seguido las recomendaciones de las guías SAGER, según la naturaleza del estudio.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
