Introducción
El pulmón destruens es una complicación poco frecuente de diversas entidades nosológicas, siendo la infección por Mycobacterium tuberculosis la causa en el 80%; se presenta en pacientes que reciben un diagnóstico y tratamiento retardado. Los hallazgos imagenológicos observados son una respuesta a los cambios compensatorios del parénquima pulmonar aun y a pesar de un adecuado tratamiento, las complicaciones tras la destrucción del pulmón afectado son diversas, en algunos casos fatales ante la presencia de hemoptisis. Asimismo, la calidad de vida del paciente se ve vulnerada al ser susceptible de infecciones oportunistas. Se presenta un caso de pulmón destruens secundario a infección por M. tuberculosis, que se diagnóstica en contexto de episodio de hemoptisis mayor.
Presentación del caso
Mujer de 27 años, originaria y residente de Tepatitlán, Jalisco, México, ama de casa durante toda su vida, soltera, perteneciente a clase baja, con carga genética para enfermedad oncológica a nivel de mama por parte de madre. Sin antecedentes exposicionales, contacto con tosedores crónicos positivo por padre, se desconoce la causa de esta. Refiere que desde la infancia padece tos, en tratamiento desde 2007 como asma sin confirmación espirométrica, tratamiento a base de broncodilatador de acción corta por razón necesaria. En octubre de 2019 acude a atención médica por pérdida de peso y tos productiva, radiografía de tórax con evidencia de caverna en ápice pulmonar izquierdo, se realiza prueba de bacilos ácido-alcohol resistentes (BAAR) seriada de expectoración con resultado positivo. Se le diagnostica tuberculosis pulmonar cavitaria y recibe tratamiento con isoniacida, rifampicina, pirazinamida y etambutol por 60 dosis; posteriormente con rifampicina e isoniacida por 45 dosis, con cultivo de expectoración sin crecimiento microbiológico al finalizar tratamiento, declarándose como caso curado en abril de 2020.
La paciente se mantiene con tos no productiva posterior a tratamiento antituberculoso, en marzo de 2023 se agrega sensación de alza térmica y en abril de 2023 hemoptisis cuantificada en 500 ml. A la exploración física, bajo peso, tórax asimétrico, vibraciones vocales ausentes e hiperresonancia en hemitórax izquierdo, con disminución de los ruidos respiratorios integrándose síndrome de rarefacción. En bioquímica: hemoglobina 9 g/dl, plaquetas 202 miles/microlitro, hematocrito 28%, leucocitos 6.7202 miles/Ál, neutrófilos 58% y glucosa 102 mg/dl. Tomografía computarizada de tórax en ventana pulmonar con herniación anterior del pulmón derecho, con tracción de mediastino hacia la izquierda, pinzamiento costal, con áreas de disminución de la atenuación que aparentan seguir trayecto bronquial sugestivos de bronquiectasias quísticas (Fig. 1).
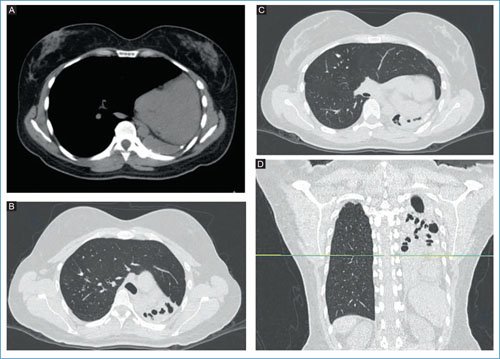
Figura 1. A: tomografía computarizada de tórax, corte axial en ventana mediastinal, con tracción de mediastino hacia la izquierda y pinzamiento de arcos costales. B y C: tomografía computarizada de tórax, cortes axiales en ventana pulmonar con herniación de parénquima pulmonar hacia izquierda, así como desplazamiento mediastinal con área de aumento de la atenuación con disminución de la atenuación en su interior sugestivos de bronquiectasias. D: corte coronal, ventana pulmonar, se aprecia ausencia de parénquima pulmonar en hemitórax izquierdo con elevación de hemidiafragma ipsilateral, así como algunas bronquiectasias de aspecto quístico y varicoso.
Se realiza broncoscopia, encontrando una disminución de diámetro de forma concéntrica de tercio medio del bronquio principal izquierdo, que no permite el paso de broncoscopio, con aparente compresión extrínseca vs. cicatrización externa al bronquio sin datos de infiltración endobronquial. En lavado bronquioloalveolar RT-PCR (reacción en cadena de la polimerasa con transcriptasa inversa) para tuberculosis y cultivo para micobacterias negativos, sin embargo, cultivo fúngico con aislamiento de Aspergillus nidulans (Fig. 2). La paciente actualmente está con adecuada evolución tras recibir manejo con itraconazol 200 mg cada 12 horas. Por riesgo de recurrencia de sangrado y colonización de bronquiectasias es valorada por el servicio quirúrgico y considerada candidata a neumonectomía izquierda, pendiente la valoración pulmonar funcional y optimización de estado nutricio de la paciente.
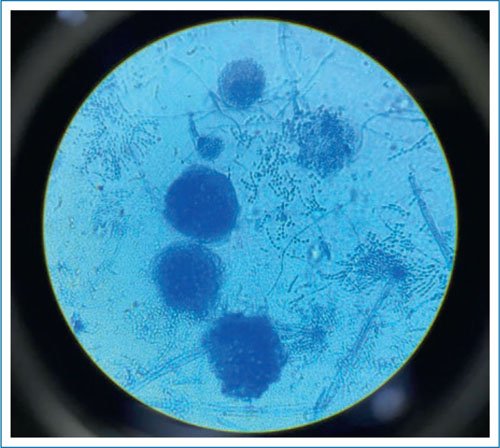
Figura 2. Aislamiento de Aspergillus nidulans con células de Hulle en tinción azul de lactofenol.
Discusión
La tuberculosis es una infección causada por el bacilo M. tuberculosis. Este agente genera un espectro de enfermedad, tanto a nivel pulmonar como extrapulmonar1. De acuerdo con el reporte de la Organización Mundial de la Salud (OMS) de 2021, se estima que el 25% de la población mundial cuenta con evidencia inmunológica de infección previa por M. tuberculosis. En México según el reporte de vigilancia epidemiológica de TB en 2022, el 78.7% de los casos corresponde a pulmón, seguido de localización miliar en 4.7% y ganglionar en tercer lugar con el 4.6%. Datos de mortalidad han informado hasta 1.4 millones de muertes a causa de este patógeno en el 2020, siendo el segundo lugar en muertes en ese año, solo seguido por el coronavirus 2 del síndrome respiratorio agudo grave (SARS-CoV-2)2.
El espectro de la enfermedad por tuberculosis dependerá de la susceptibilidad del huésped, aumentando el riesgo ante la presencia de diabetes, alcoholismo o VIH. Existen tres formas de la enfermedad a nivel pulmonar3 (Tabla 1).
Tabla 1. Formas patológicas de la infección pulmonar por Mycobacterium tuberculosis y sus manifestaciones imagenológicas
| Primaria | Aparece como consolidación, principalmente en lóbulos superiores, derrame pleural, enfermedad miliar, linfadenopatías hiliares y mediastínicas |
| Posprimaria | Enfermedad cavitaria y/o nodular |
| Latente | Paciente con pruebas de tuberculina o pruebas moleculares sin hallazgos imagenológicos o clínicos sugestivos de tuberculosis primaria o posprimaria |
En años recientes, el término de enfermedad postuberculosa ha cobrado mayor relevancia, derivado del impacto de las secuelas a largo plazo que dicha infección puede generar a pesar de recibir un tratamiento adecuado. Por ello se ha definido la enfermedad postuberculosa como anormalidades respiratorias crónicas, con o sin síntomas asociados, atribuibles a infección pulmonar previa. La prevalencia es variable, ya que no existen suficientes estudios para llegar a un consenso, mencionándose fluctuar entre el 18-87%, entrando en este reciente concepto el pulmón destruens4.
El pulmón destruens o pulmón destruido se define como una combinación de destrucción del parénquima pulmonar y pleural manifestado radiológicamente como cavitaciones, bronquiectasias, pérdida de volumen pulmonar y herniación mediastinal hacia el lado afectado5. Se considera una afección común en países con sistemas de salud subdesarrollados. La principal causa es la infección por M. tuberculosis (80% de los casos), en menor proporción la neumonía necrotizante y estadios finales de bronquiectasias6, el desarrollo de esta secuela se presenta en el 1.3% de los pacientes a pesar del tratamiento instaurado7.
Los factores de riesgo identificados en series de casos son pacientes hombres, edad media de presentación de 55 años, diagnóstico de tuberculosis durante la infancia o adolescencia5. Los pacientes con esta afección suelen presentarse inicialmente asintomáticos y finalmente desarrollar sintomatología crónica con tos productiva en ocasiones purulentes, hemoptisis, fiebre y disnea. A la exploración física puede encontrarse asimetría en tórax a expensas de hemitórax afectado, con disminución y horizontalización de los espacios intercostales8. Imagenológicamente en radiografía de tórax posteroanterior pueden observarse radioopacidad difusa en hemitórax afectado, desviación mediastínica ipsilateral, bronquiectasias quísticas, cavitaciones, mientras que en la proyección lateral se ha descrito hiperclaridad retroesternal en relación con hiperinsuflación del pulmón contralateral9.
Los hallazgos tomográficos de acuerdo con Shital et al. se describen en la figura 310. Series de casos han evidenciado predilección de afección de pulmón izquierdo aproximadamente en el 58.1% de los casos, la herniación del pulmón sano en el 92% de los casos es anterior a mediastino involucrando lóbulo superior y medio, la herniación posterior con involucro del lóbulo inferior se presenta en el 85% y menos común la afección simultánea en el 77%5,11. La predilección de afección hacia el lado izquierdo es debido a la anatomía bronquial, siendo el bronquio principal izquierdo más alargado, estrecho y horizontalizado en comparación con el derecho, lo cual empeora el drenaje de secreciones12.
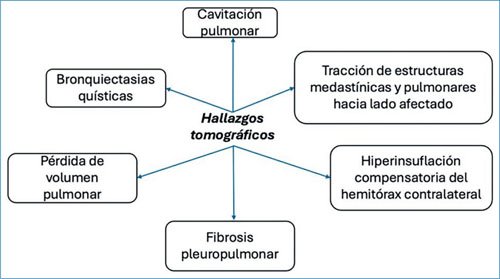
Figura 3. Hallazgos tomográficos de pulmón destruens.
El manejo quirúrgico se reserva para pacientes con complicaciones como hemoptisis, fístula broncopleural o desarrollo de empiema. Dentro de las opciones que se encuentran descritas está la neumonectomía, pleuroneumomnectomía, reparación de fístula broncopleural más neumonecnomía. La indicación de cada una de estas es controversial y no existe un consenso. En una serie de casos de 172 pacientes la pleuroneumonectomía se realizó en pacientes con pulmón destruido y adhesiones pleurales, mientras que ante ausencia de empiema o fístula broncoplerual se prefiere la neumonectomía; y en caso de fístula broncoplerual, la reparación de fístula broncopleural más neumonectomía es la opción seleccionada13. La mortalidad operatoria global para la neumonectomía se reporta en el 4%, siendo las complicaciones más comúnmente presentadas la fístula broncopleural (12%) y el empiema (32%). Se consideran contraindicaciones absolutas FEV1 (volumen espiratorio forzado en el primer segundo 2 l y capacidad de difusión de monóxido de carbono < 60%.
La coinfección se ha descrito en pequeñas series de casos reportándose hasta en el 46.1% de los pacientes, siendo los agentes mayor observados gramnegativos como Pseudomona aeruginosa, Haemophilus influenzae y en menor proporción infecciones fúngicas14.
Conclusiones
En el presente caso se presenta una de las complicaciones menos comunes de la infección por M. tuberculosis, el pulmón destruens o destruido. Entidad poco conocida por el tratamiento antituberculoso oportuno establecido al momento del diagnóstico, con hallazgos imagenológicos característicos, cuyas recomendaciones de manejo aún está en estudio.
Financiamiento
La realización del presente trabajo no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
