Introducción
La apnea obstructiva del sueño (AOS) es una condición exclusiva del sueño. Se define como colapsos parciales o totales en la vía aérea superior (VAS), asociados a hipoxemia, hipercapnia, hipoventilación y/o microalertamientos, ronquido, sueño fragmentado no reparador y somnolencia diurna excesiva (SDE), entre otros síntomas. Se correlaciona con aumento en riesgo cardiovascular, alteraciones metabólicas, cognitivas y empeoramiento de la calidad de vida de los afectados1,2. La AOS presenta una prevalencia global del 4-30%3.
Según la fisiopatología, características polisomnográficas y presentación clínica, se han identificado diversos fenotipos de AOS. Uno de ellos, conocido como AOS postural (POSA, por sus siglas en inglés), describe a pacientes cuyos eventos respiratorios obstructivos son más frecuentes en posición supina. Se presenta en poblaciones caucásicas y asiáticas, en jóvenes, delgados, con menor índice de masa corporal (IMC), presión arterial más baja y un índice de apnea-hipopnea (IAH) menos grave; experimentan pocos despertares y ronquidos, con una mejor duración y eficiencia del sueño4,5. La prevalencia de POSA se encuentra entre el 50 y 60% de los pacientes con AOS6.
El tratamiento para la POSA incluye la terapia de presión positiva (PAP), dispositivos de avance mandibular (DAM), cirugía de la vía aérea superior, algunos medicamentos y terapia posicional (TP). Estos tratamientos son específicos y/o complementarios según el fenotipo y endotipo predominante en cada paciente con notable variabilidad en su eficacia. Esta revisión narrativa de la literatura tiene como objetivo la descripción y reconocimiento médico de las características de pacientes con POSA.
Historia y definición de la apnea obstructiva del sueño postural
La POSA se considera un fenotipo específico de AOS. Se define por la presentación de apneas e hipopneas de forma exclusiva o predominantemente significativa en una posición determinada, es decir, la peor posición (Fig. 1, Tabla 1); aunque los valores específicos para el diagnóstico de este trastorno del sueño varían en la literatura publicada.
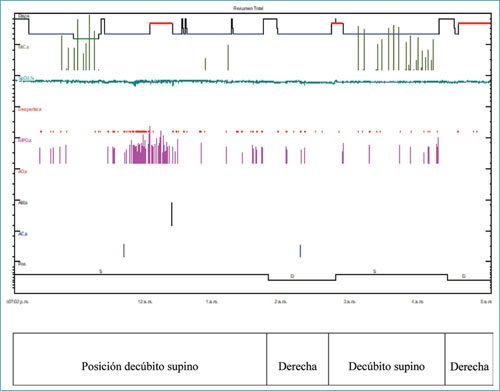
Figura 1. Apnea obstructiva del sueño postural. Polisomnografía con claro predominio de apneas e hipopneas obstructivas durante el decúbito supino independiente de la fase del sueño.
Tabla 1. Apnea obstructiva del sueño postural (POSA) distribución de las posiciones corporales
| Posición | Duración (min) | Sueño (%) | MOR (%) | Desaturación de oxígeno (eventos) | Índice de apnea hipopnea (n.º/h) |
|---|---|---|---|---|---|
| Supino | 307.8 | 94.4 | 8.6 | 117 | 17.1 |
| Derecha | 96.7 | 86.3 | 33.6 | 21 | 4.3 |
| Izquierda | |||||
| Prono |
Se observa un índice de apnea hipopnea alterado en la posición decúbito supina.
MOR: sueño con movimientos oculares rápidos.
Cartwright fue el primero que sugirió diferenciar entre pacientes con POSA y AOS no postural (no-POSA), definiendo la POSA de forma arbitraria como la presencia de 50% o más en el IAH entre las posiciones supina y no supina7. Desde entonces diferentes autores han planteado múltiples modificaciones, con el fin de ser más específicos en los criterios para el diagnóstico y mejorar la eficacia de las terapias utilizadas (Tabla 2)7–12.
Tabla 2. Definiciones de la apnea obstructiva del sueño postural
| Autor | Año | Definición |
|---|---|---|
| Cartwright7 | 1984 | IAH total > 5/h, diferencia del 50% o más en el IAH entre la posición supina y no supina |
| Marklund et al.8 | 1998 | IAH ≥ 10/h en supino + IAH lateral < 10/h en lateral |
| Permut’s9 | 2005 y 2010 | IAH < 5/h en la posición no supina sumado a una disminución del IAH > 50% entre la posición supina y no supina. Diferencia entre apnea postural predominante en supino (IAH ≥ 5/h en posición no supina) y apnea postural exclusiva en supino (IAH < 5/h en posición no supina) |
| Bignold et al.10 | 2011 | IAH total ≥ 15/h, IAH supino ≥ al doble que el IAH no supino, IAH < 15/h en no supino. Mínimo 20 minutos de sueño en posición supina y lateral. |
| Levendowski et al.11 | 2014 | IAH total/IAH en no supino > 1.5 |
| Frank et al.12 | 2015 | Introduce 3 categorías (APOC) teniendo en cuenta mejor y peor posición. Mínimo 10% del tiempo total de sueño en la mejor y peor posición |
APOC: Amsterdam Positional OSA Classification; IAH: índice de apneas e hipopneas/hora.
Bignold et al. definen la POSA como un IAH total igual o mayor a 15/h, el doble de eventos en supino vs. la posición no supina, con un IAH no supino igual o menor a 15/h, siempre y cuando se cuantifiquen 20 minutos o más de sueño en las posiciones evaluadas10; esta definición específica y acorde con la Academia Americana de Medicina del Sueño (AASM)13.
Frank et al. suman las definiciones de mejor y peor posición asociado a un tiempo mínimo de registro por posición12, lo que se complementa en 2016 con la Clasificación de Ámsterdam de Apnea Postural (APOC, por su sigla en inglés), enfocados en mejorar la selección de pacientes y por ende la eficacia de la terapia de reentrenamiento posicional (TRP) con tres categorías6 (Tabla 3).
Tabla 3. Clasificación de Ámsterdam de Apnea de Sueño Postural y su impacto en la selección de tratamiento con terapia de reentrenamiento posicional
| Clasificación | Definición | Implicación en tratamiento |
|---|---|---|
| APOC I | IAH en posición más favorable durante el sueño menor a 5/h (POSA exclusiva) | Terapia o reentrenamiento posicional como monoterapia |
| APOC II | IAH en posición más favorable durante el sueño disminuye la gravedad de la AOS | Terapia o reentrenamiento posicional como coadyuvante |
| APOC III | IAH total ≥ 40, con reducción de mínimo 25% del IAH en posición más favorable | Considerar terapia o reentrenamiento posicional como coadyuvante |
APOC: Amsterdam Positional OSA Classification.
Adaptada de Berri et al.13
Epidemiología y características clínicas
La AOS es la entidad más prevalente de los trastornos respiratorios del dormir, afecta al 12.5% de hombres y el 5.9% de mujeres en la población general, el 49.7% de hombres y el 23.4% de mujeres mayores de 40 años tiene un IAH > 15/h14. Ahora bien, la prevalencia de POSA es variable en relación con la edad, etnia e IAH de la población estudiada y los criterios que se escojan para el diagnóstico. Se estima, sin embargo, que la POSA predominante (POSAp) se encuentra entre el 50 y 60%15–17, mientras que la POSA exclusiva (POSAe) se presenta entre el 20 y 35%11,18 (Fig. 2).
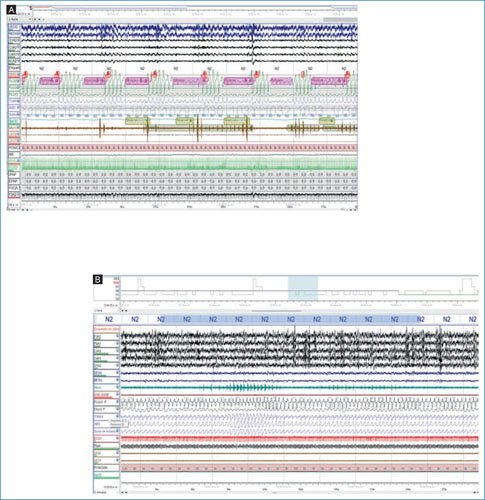
Figura 2. Apnea obstructiva del sueño posicional exclusiva. Se pueden observar dos épocas de 5 minutos durante estudio de polisomnografía basal. A: paciente en posición supina presentando ronquido e hipopneas asociados a desaturación y microalertamientos en N2. B: paciente en posición decúbito lateral izquierdo con persistencia de ronquido, sin eventos respiratorios obstructivos ni desaturación en N2.
Los estudios sugieren una mayor prevalencia de POSA en la población asiática, un 67-75%19,20, así como en pacientes jóvenes, delgados y con menos comorbilidades15,16,21; el promedio de edad es de 49.5-52.9 años frente a 54.9-59.2 años9,16. Existe también una proporción inversa entre la gravedad de la AOS y la prevalencia de POSA. Mador et al. evidenciaron una prevalencia de POSA en AOS leve del 49.5%, en AOS moderado del 19.4% y en AOS grave del 6.5%19. La POSA es más frecuente en hombres que en mujeres, con una proporción de 11.1:1 para los distintos grados de gravedad de la AOS, y para AOS leve y moderado 2.6:1; esta discrepancia se puede explicar en la mayor cantidad de hombres con AOS grave18,22.
Los pacientes con POSA tienden a presentar un IMC más bajo 29.3-31.6 kg/m2 vs. aquellos con AOS no postural 31.9-38 kg/m2 9,16,18; la diferencia en IMC es notable en pacientes con POSA exclusiva incluso cuando se controla el factor de IAH; quienes también exhiben circunferencias del cuello y cintura menor, clasificación de Mallampati más favorable, menos prevalencia de hipertensión arterial, mayor nadir de saturación de oxígeno y menores niveles de glucemia, datos que además son factores de riesgo independiente para la no POSA9,23.
En la clínica los pacientes con no POSA muestran mayor puntaje en la escala de somnolencia de Epworth24, cuestionarios de STOP y STOP-Bang25, y en el cuestionario de Berlín18,26, probablemente asociado a cifras mayores de IAH, índice de desaturación, microalertamientos, y disminución en las etapas N3 y R, con menor eficiencia de sueño7,20. Por otra parte, el ronquido en los pacientes que presentan POSA se reporta más frecuente y de mayor intensidad en la posición supina27,28, hecho que se debe tener en cuenta a la hora de seleccionar la TP, como única o combinada, en aquellos pacientes que persisten roncando en las posiciones favorables.
Fisiopatología
Siendo la POSA una variante fenotípica de la AOS, tiene múltiples factores en su patogénesis, que incluyen las condiciones anatómicas, la presión critica de cierre (Pcrit), el volumen pulmonar y tracción traqueal, la acción de los músculos dilatadores de la VAS, la estabilidad ventilatoria y el umbral de despertar29. La interacción y el equilibrio entre estos factores, en diferentes etapas y momentos, es determinante en la aparición de los eventos, y su entendimiento es clave en la búsqueda de tratamientos específicos.
Anatomía
El tamaño, forma y posición de las estructuras óseas (maxila, mandíbula, vértebras cervicales) y de los tejidos blandos (válvula nasal, cornetes, adenoides, paladar blando, úvula, músculos palatofaríngeos y palatogloso, amígdalas palatinas, amígdalas linguales, lengua, epiglotis, cojinetes grasos), así como la forma y características de tono de la VAS influencian el colapso de la VAS en los pacientes con AOS. Este hecho es especialmente cierto en la posición supina, como se ha demostrado mediante imágenes estáticas y dinámicas durante la vigilia y el sueño, en estudios que observan diferentes posiciones corporales y rotación cefálica, a pesar del obstáculo causado por el uso de diferentes métodos de evaluación, características de la población y etapas del sueño en las que se realiza la evaluación30–32.
Los pacientes sin AOS normalmente tienen cambios en el área de la VAS cuando cambian de sedestación al decúbito supino pero no presentan cambios de decúbito supino a lateral32, a diferencia de los pacientes con AOS, quienes en decúbito supino presentan una pequeña pero significativa disminución en el espacio anteroposterior, retropalatal y en el área a nivel de orofaringe e hipofaringe33. Mientras que los pacientes con POSA presentan una posición más posterior de la mandíbula y una mayor área lateral en el espacio retropalatal, y de la orofaringe e hipofaringe34–37. Aunque hasta el momento se han realizado pocos estudios para comparar el comportamiento de la VAS en las endoscopias bajo sedación, se ha evidenciado menor presentación de colapso concéntrico retropalatal y mayor colapso a nivel de epiglotis, más que en la base de lengua en los pacientes con POSA38,39.
Se ha planteado la hipótesis de que el aumento en el diámetro lateral en orofaringe e hipofaringe evidenciado en los pacientes con POSA disminuye la posibilidad de eventos obstructivos en la posición lateral, que compensa el área anteroposterior disminuida característica de los pacientes con AOS, lo que también se asocia a mejores condiciones en otros factores como los volúmenes pulmonares.
Se discute también si la resistencia nasal derivada de la obstrucción mecánica de la nariz, al aumentar la colapsabilidad del «tubo» de la VAS, estaría implicada en cómo un paciente no POSA se podría convertir en un paciente POSA una vez tratados esos puntos obstructivos, siendo esto una forma eficiente como manejo alternativo a las terapias de PAP.
Volúmenes pulmonares
El volumen pulmonar es un factor importante en la generación de la AOS, y tiene relación con la estabilidad de las estructuras de la VAS por medio de la tracción caudal que ejerce la tráquea, así como con la presión crítica de cierre de la VAS (Pcrit)40–42. En el ser humano el cambio de bipedestación a decúbito supino implica una caída de la capacidad residual funcional (CRF), la capacidad pulmonar total, el volumen de reserva espiratoria (VRE) y la capacidad vital, sin cambios en el volumen residual43–45. Estos volúmenes también son afectados por el IMC, así, los pacientes con IMC 25-30 kg/m2 disminuyen linealmente la CRF y el VRE cuando pasan de estar sentados al decúbito supino46. Aún falta información respecto a estos volúmenes en cambios de posición de decúbito lateral a supino47–49. Como se dijo los cambios en los volúmenes pulmonares, afectan la estabilidad de la VAS durante el sueño en la posición supina43–46,50,51. Stanchina et al. demostraron en 19 adultos jóvenes normales que una reducción de 600 ml al final del volumen espiratorio aumenta el punto crítico de cierre faríngeo en 1.1 cmH2O, determinando que la VAS se vuelva colapsable pese a un aumento en la activación del músculo geniogloso41, comparable a la observación de Tagaito et al., en la que el aumento en el volumen de fin de espiración en 750 ml reduce el punto crítico de cierre faríngeo en 1.2 cmH2O52. Stadler et al., utilizando un manguito alrededor del abdomen, evidenciaron que el aumento de la presión intraabdominal durante el sueño en obesos (media de IMC: 34.5 kg/m2) produce una caída del volumen al final de la espiración de 530 ml y aumento en el punto crítico de cierre faríngeo en 1.4 cmH2O, demostrando la interacción entre el aumento del IMC, la disminución de volúmenes pulmonares y el aumento de la colapsabilidad de la VAS53.
Presión crítica de cierre
La afectación anatómica funcional de la VAS es medida por la Pcrit54,55. Tener una Pcrit supraatmosférica o «positiva» hace más propenso a tener AOS, a diferencia de las Pcrit «negativas», es decir, con presiones intraluminales negativas o de succión56–58. La Pcrit varía por muchos factores, desde las configuraciones de los tejidos óseos y blandos, el IMC y la etapa del sueño, hasta la posición del cuerpo y la cabeza59,60. Hasta el momento no se han realizado estudios específicos valorando la Pcrit en pacientes con AOS y POSA; sin embargo, se presume que los pacientes con POSA tienen cambios más significativos en la Pcrit en las diferentes posiciones, asociados a condiciones anatómicas predisponentes y cambios importantes en los volúmenes pulmonares.
Terapia y reentrenamiento posicional
La terapia con PAP sigue siendo la referencia de tratamiento de la AOS, sin embargo han surgido nuevos abordajes terapéuticos y en el caso de los pacientes con POSA se han descrito varios tipos de tratamientos: terapia PAP, DAM, manejo quirúrgico, TP y terapia y reentrenamiento posicional (TRP)61,62. La TP es el manejo de elección para estos pacientes, sea como monoterapia o en combinación con otras estrategias terapéuticas; consiste en evitar que el paciente adopte la peor posición mientras duerme, habitualmente el supino, mediante diferentes métodos.
La primera descripción registrada en 1984 en la literatura se encuentra en una carta escrita por la esposa de un paciente. En ella relata cómo logró mitigar los ronquidos de su esposo al coser un bolsillo en la parte posterior de la camisa del pijama e insertar una pelota de tenis en dicho bolsillo. Se conoce como «la técnica de la pelota de tenis» (TPT). Aunque informes de casos pequeños han demostrado que esta técnica es efectiva para evitar la posición supina, su baja adherencia a largo plazo se atribuye a la incomodidad, el dolor y los múltiples despertares que puede ocasionar63–65.
Se han propuesto modificaciones utilizando objetos como almohadas especiales y chalecos con cojines66–68, pero persiste una baja adherencia a largo plazo y la incapacidad para medir de manera objetiva el tiempo real de uso y la posición no supina con estos tratamientos. En respuesta a esta problemática, surge la TRP, cuyo propósito es inducir una reubicación en una posición favorable mediante dispositivos colocados en diferentes partes del cuerpo que generan una vibración sutil. Este enfoque ha demostrado ser más eficiente, efectivo y cómodo a largo plazo12,69,70. La TRP puede ser curativa en algunos casos de pacientes con POSAe según la clasificación de APOC dentro de la cual los APOC I son los verdaderamente posicionales, y puede ser coadyuvante en los demás casos.
De Vries et al.63 evaluaron la efectividad de la TP, incluyendo 53 participantes de los cuales a 40 se les realizó una polisomnografía (PSG) control y usando una banda comercial en el pecho o con dispositivo casero, se halló una disminución significativa en el IAH de pacientes con POSA (IAH medio:14.5-5.9/h; p < 0.001), con un seguimiento de 12 semanas, lo que corroboró reportes de casos previos.
Aunque hay pocos estudios62,63,65, se demuestra pobre adherencia a largo plazo de este tipo de terapia. Es así como De Vries et al. describen que el 65% de los pacientes a 13 meses han descontinuado el tratamiento63. Oksenberg et al. reportan una adherencia a 6 meses del 38%62, Bignold et al. evidencian un uso de TP con TPT a 30 meses menor del 10%65. En 2012 Heinzer et al.71 evaluaron el uso real de TP con TPT modificado en conjunto con actigrafía donde evidenciaron un uso objetivo en 16 pacientes durante 3 meses: de 8 horas en promedio (rango: 3.8-10.2 h), 10 pacientes usaron más del 80% del tiempo el dispositivo y 13 más del 60%. Lo anterior muestra claras desventajas de la TPT frente a otras TP y en especial la TRP.
Terapia de reentrenamiento posicional o nueva terapia posicional
Las nuevas tecnologías aplicadas a esta área han llevado a varias publicaciones en la última década describiendo la eficacia y seguimiento a largo plazo de pequeños dispositivos vibrátiles con acelerómetros integrados, que se ubican en tórax anterior, región cervical y frontal, cuyo objetivo es indicar al paciente que debe cambiar de posición, por medio de vibraciones crecientes, constituyendo la TRP67,72–75. Sus ventajas incluyen mejor adherencia, mayor comodidad, manejo de diferentes posiciones y datos objetivos de seguimiento. Algunos de ellos cuentan con aprobación de la Food and Drug Administration (FDA) y tienen estudios comparativos con otras terapias para AOS74–76.
Bignold et al.10 valoraron el uso de un dispositivo vibrátil para el tratamiento de POSA en 15 pacientes. Realizando un tratamiento cruzado donde evidenció una reducción significativa del tiempo en supino y del IAH (de 25 a 13.7/h). Ravesloot et al.27 demostraron la capacidad de un dispositivo de TRP para disminuir el IAH total y el tiempo en supino durante el sueño en 31 pacientes con POSA luego de 4 semanas de tratamiento. En este estudio se evidenció una mejoría en la SDE y en la calidad de sueño. Datos corroborados a los 6 meses por van Maanen69 y de forma más reciente los mismos resultados se observan en un estudio controlado aleatorizado realizado por Laub et al. en 52 pacientes con POSA72.
Levendowski et al.11 demostraron en 30 pacientes con POSA una reducción en el IAH de 24.7-14.7/h a 7.5-7.7/h (p < 0.00001) después de 4 semanas de usar un dispositivo vibrátil en el cuello. En este mismo estudio se evidencia que la TP redujo significativamente los trastornos respiratorios del sueño y mejoró significativamente la calidad del sueño, además de reducir moderadamente los síntomas en los distintos grupos según la gravedad de la AOS.
Hidalgo Armas et al.77, en un estudio observacional prospectivo con intervención, usan un dispositivo vibrátil frontal (n = 128 pacientes), evaluando varios parámetros por 12 semanas. En dicho estudio se evidencia una reducción significativa del IAH de 30.6/h a 20.4/h (p < 0.001), así como disminución en el tiempo en supino y aumento en el tiempo total de sueño, y estadios N3 y REM. Lo anterior demuestra como la TRP mejora varios parámetros como son el IAH, el tiempo en supino, la calidad de vida, y la SDE en los pacientes con POSA, con una adherencia superior a la TP convencional, evidenciando adherencias del 92.7% a 1 mes, 89% a 3 meses, 64.4% a 6 meses y 82% a 12 meses72,73.
Srijithesh et al.78, en un estudio controlado aleatorizado con cruce de no inferioridad (n = 40), compararon durante 16 semanas un dispositivo de TRP (Night shift) con un dispositivo de presión positiva continua automático (auto-CPAP), realizando un cruce de tratamiento a las 8 semanas. El parámetro principal fue la SDE, y la predilección de tratamiento por el paciente y datos de la PSG fueron parámetros secundarios, sin embargo el estudio no fue conclusivo porque la SDE no cumplió con el valor predeterminado de no inferioridad. Respecto a otros parámetros, se evidenció que los pacientes preferían el tratamiento con auto-CPAP (60%) frente a TRP (20%), y el 20% no prefería ninguna de las dos opciones. El IAH residual fue menor con CPAP que con TRP (0 ± 3.2 vs. 13.0 ± 13.8/h, respectivamente; p = 0.001).
Estos hallazgos no difieren de los encontrados por Berry et al.79, quienes incluyeron 117 pacientes y encontraron que, aunque la arquitectura del sueño fue igual para ambos tratamientos (APAP y el dispositivo médico usado para TRP), los microdespertares fueron menos en el brazo de TRP, mientras que el IAH fue menor en el brazo de APAP (IAH 7.29 vs. 3.71), manteniendo una mejor saturación de oxígeno. Cabe destacar que la diferencia en el IAH fue un factor presupuestado en ambos estudios y que en general la eficacia relativa de los dispositivos TRP fue similar al CPAP, manteniendo un IAH < 10/h.
Benoist et al.74 publicaron los resultados de su estudio multicéntrico aleatorizado controlado prospectivo que comparaba un DAM con un dispositivo médico utilizado para la TRP en pacientes con POSA leve y moderada. En este estudio se asignaron aleatoriamente 99 pacientes a DAM o TRP, y se analizaron los datos de 81 al finalizar el seguimiento de 3 meses. En cuanto al IAH después de 3 meses de tratamiento, no se observaron diferencias significativas (TRP 13.0-7.0/h, DAM 11.7-9.1/h). La adherencia promedio al tratamiento fue mayor para TRP (88.4 vs. 60.5%). Los autores concluyeron que ambos tratamientos son comparables en cuanto a efectividad y adherencia en pacientes con POSA leve y moderada. Es importante señalar que los pacientes con DAM informaron más efectos secundarios durante el seguimiento en comparación con los pacientes que utilizaron TRP (26.8 vs. 13.4%), un hecho relevante ahora que el DAM se considera más como una terapia temporal debido a sus posibles efectos adversos en la oclusión y salud dental.
Se han realizado algunos estudios con respecto a TRP como terapia combinada con DAM o posterior a manejo quirúrgico de la AOS en pacientes con POSA79,80. En estos se observan algunas aplicaciones adicionales de TRP, sin embargo no se cuenta con la evidencia suficiente por el momento para dar conclusiones al respecto. Este es un campo para profundizar.
Finalmente, ALQarni et al., en una revisión sistemática de la literatura y metaanálisis identificaron 1,119 estudios, de los cuales 18 cumplieron con los criterios de inclusión (10 ensayos controlados aleatorizados y 8 estudios de cohortes). El uso de TP vibrotáctil redujo significativamente el IAH en el seguimiento en comparación con el inicio (diferencia media –9.19 eventos/h; IC 95%: –11.68 a –6.70%; p < 0.00001). El porcentaje de tiempo en posición supina (%T supino) también se redujo significativamente (diferencia media –32.79%; IC 95%: –38.75 a –26.83%; p < 0.00001). Los cambios porcentuales en el IAH y %T supino fueron del 43 y 70%, respectivamente. Los resultados secundarios incluyeron somnolencia diurna, calidad de vida e índices de sueño. Estos mostraron cambios mínimos, aunque el seguimiento fue breve. Los autores concluyen que la TP vibrotáctil fue efectiva en reducir el tiempo pasado en la posición supina y la gravedad de la AOS, así como la somnolencia diurna; sin embargo, este último hallazgo no alcanzó una diferencia estadísticamente significativa81.
Conclusiones
La variante posicional de la apnea del sueño (POSA) es altamente prevalente en la población con AOS, independiente de la gravedad del IAH. La TP y la TRP constituyen una oportunidad de tratamiento único o como coadyuvante que ha ganado aceptación entre pacientes y médicos por su eficacia, versatilidad y comodidad, sin embargo, aún se requieren más estudios que avalen su eficacia y seguridad.
Financiamiento
La realización del presente trabajo no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han obtenido la aprobación del Comité de Ética para el análisis de datos clínicos obtenidos de forma rutinaria y anonimizados, por lo que no fue necesario el consentimiento informado. Se han seguido las recomendaciones pertinentes.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
