Introducción
La tuberculosis (TB) sigue siendo la principal causa de muerte por un solo agente infeccioso, con un estimado de 1.5 millones de defunciones para el año 2020. En 2023, México reportó una incidencia de 29 casos de TB por cada 100,000 habitantes, de acuerdo con la Organización Mundial de la Salud1. Las tasas estatales por 100,000 habitantes incluyeron: Baja California 47.92, Sonora 38.35, Chihuahua 33.68 y Zacatecas 21.312,3.
Aunque existen plataformas epidemiológicas nacionales, México carece de datos sistematizados y actualizados sobre la prevalencia de TB, su asociación con variables clínicas y epidemiológicas, comorbilidades relevantes y desenlaces de los pacientes durante los últimos cinco años. La información epidemiológica situacional permite caracterizar a los pacientes dentro de un área geográfica y estimar contactos y posibles cadenas de transmisión para seguimiento. Identificar factores de riesgo para el desarrollo de TB en estudios representativos ayuda a reconocer a los individuos con mayor probabilidad de enfermar y respalda medidas preventivas y un diagnóstico clínico oportuno.
Zacatecas, un estado en la región centro-norte de México, ha concentrado aproximadamente el 10% de los casos anuales de TB en los últimos cinco años, prácticamente duplicando los reportes previos4. Por ello, comprender los factores asociados con el incremento en la diseminación, así como delinear la supervivencia y las características que contribuyen a desenlaces adversos, es de gran relevancia.
El objetivo del presente estudio fue identificar los factores epidemiológicos asociados con la TB, los desenlaces clínicos y la supervivencia entre los pacientes atendidos en el sistema IMSS en Zacatecas durante 2019-2023.
Material y métodos
Se llevó a cabo una cohorte retrospectiva para determinar la supervivencia a cinco años y los predictores de mortalidad en TB, tras la autorización del Comité Local de Investigación en Salud y Ética del IMSS (registro R-2024-3301-031). Se identificaron todos los pacientes adultos (≥ 18 años) que recibieron atención por TB en el IMSS Zacatecas entre enero de 2019 y diciembre de 2023. La inclusión requirió al menos una muestra clínica con cultivo positivo para micobacterias o una prueba de amplificación de ácidos nucleicos positiva (GeneXpert). Las muestras incluyeron esputo, líquido cefalorraquídeo, líquido peritoneal (ascitis), orina y tejidos quirúrgicos (p. ej., ganglios linfáticos, mucosa intestinal) con granulomas positivos en tinción de Ziehl-Neelsen. Se excluyeron pacientes con expedientes clínicos incompletos o sin seguimiento.
De 145 casos iniciales, 25 fueron excluidos debido a datos clínicos inespecíficos o ausencia de estudios confirmatorios de laboratorio o imagen. La muestra final incluyó un total de 125 pacientes con hasta cinco años de seguimiento (media: 32 meses; rango: 1-65 meses). Los objetivos primarios fueron las complicaciones y la muerte. Se evaluó la supervivencia de todos los pacientes, identificándose 22 defunciones frente a 103 sobrevivientes, y se utilizó el tiempo desde el inicio de la enfermedad hasta la última evaluación para estimar los parámetros de supervivencia.
Las variables categóricas se analizaron según el estado de supervivencia y se compararon con las características sociodemográficas y clinicopatológicas. Se generaron estadísticas descriptivas. La normalidad se evaluó para determinar el uso de medidas de dispersión o frecuencias/porcentajes. Para las variables categóricas, se calcularon riesgos relativos (RR); para las variables numéricas, se aplicó la prueba t de Student o equivalentes no paramétricos según correspondiera. La supervivencia se analizó mediante métodos de Kaplan-Meier, y los factores asociados con supervivencia se evaluaron con regresión de riesgos proporcionales de Cox. Un valor de p bilateral < 0.05 se consideró estadísticamente significativo. Los análisis se realizaron con SPSS v25.
Resultados
Características descriptivas
Entre los 125 pacientes, el 54.4% fueron hombres; la edad media fue de 47.5 ± 18.5 años. El 51.2% reportó estar empleado; el 44.8% tenía un nivel socioeconómico medio–bajo y el 35.2% uno bajo. La mayoría de los casos procedían de la capital del estado (43.2%) y del municipio conurbado de Guadalupe (36%).
Las exposiciones relevantes incluyeron tabaquismo (24%), alcoholismo (17.6%), exposición a biomasa (8%), exposición minera (5.6%), consumo de drogas ilícitas (4.8%), antecedente de TB (4.8%), contacto domiciliario con un caso de TB (3.2%) y hacinamiento (2.4%) (Tabla 1).
Tabla 1. Condiciones diagnósticas y antecedentes clínicos en pacientes con TB atendidos en IMSS Zacatecas (2019-2023)
| Estatus | Defunción | RR | IC 95% | ||
|---|---|---|---|---|---|
| Total (n = 125) Frecuencias (%) | Sí (n = 22) Frecuencias (%) | No (n = 103) Frecuencias (%) | Inferior/Superior | ||
| Hacinamiento | 3 (2.4) | 3 (13.6) | 0 (0.0) | 6.421 | 4.247-9.705 |
| Exposición a biomasa | 10 (8.0) | 3 (13.6) | 7 (6.8) | 2.165 | 0.513-9.132 |
| Exposición a mina | 7 (5.6) | 1 (4.5) | 6 (5.8) | 0.770 | 0.087-6.735 |
| Contacto con caso de TB | 4 (3.2) | 0 (0.0) | 4 (3.9) | 1.222 | 1.123-1.329 |
| Alcoholismo | 22 (17.6) | 8 (36.4) | 14 (13.6) | 3.633 | 1.289-10.23 |
| Tabaquismo | 30 (24.0) | 12 (54.5) | 18 (17.5) | 5.667 | 2.124-15.11 |
| Drogas | 6 (4.8) | 2 (9.1) | 4 (3.9) | 2.475 | 0.424-14.44 |
| Tuberculosis previa | 6 (4.8) | 0 (0.0) | 6 (5.8) | 1.227 | 1.126-1.336 |
| Diabetes | 27 (21.6) | 6 (27.3) | 21 (20.4) | 1.464 | 0.510-4.199 |
| Virus de inmunodeficiencia humana (VIH) | 7 (5.6) | 2 (9.1) | 5 (4.9) | 1.960 | 0.354-10.82 |
| Hipertensión (HTA) | 33 (26.4) | 6 (27.3) | 27 (26.2) | 1.056 | 0.374-2.974 |
| Artritis reumatoide (AR) | 10 (8.0) | 1 (4.5) | 9 (8.7) | 0.497 | 0.059-4.141 |
| Enfermedad pulmonar obstructiva crónica (EPOC) | 7 (5.6) | 2 (9.1) | 5 (4.9) | 1.960 | 0.354-10.82 |
| Enfermedad renal crónica (ERC) | 3 (2.4) | 0 (0.0) | 3 (2.9) | 1.220 | 1.122-1.325 |
| Desnutrición | 10 (8.0) | 5 (22.7) | 5 (4.9) | 5.765 | 1.506-22.06 |
| Neoplasias | 5 (4.0) | 0 (0.0) | 5 (4.9) | 1.224 | 1.124-1.332 |
| Depresión | 6 (4.8) | 2 (9.1) | 4 (3.9) | 2.475 | 0.424-14.44 |
| Trastorno metabólico/mal control metabólico | 9 (7.2) | 0 (0.0) | 9 (8.7) | 1.234 | 1.130-1.347 |
| Inmunosupresión | 11 (8.8) | 3 (13.6) | 8 (7.8) | 1.875 | 0.455-7.721 |
| Tratamiento para la hipertensión | 34 (27.2) | 6 (27.3) | 28 (27.2) | 1.004 | 0.357-2.824 |
| Tratamiento con insulina | 6 (4.8) | 3 (13.6) | 3 (2.9) | 5.263 | 0.987-28.06 |
| Tratamiento con corticoesteroides | 11 (8.8) | 4 (18.2) | 7 (6.8) | 3.048 | 0.807-11.49 |
| Tratamiento con biológicos | 8 (6.4) | 1 (4.5) | 7 (6.8) | 0.653 | 0.076-5.594 |
| Tratamiento con antidepresivos | 4 (3.2) | 2 (9.1) | 2 (1.9) | 5.050 | 0.671-37.98 |
| Hemodiálisis | 3 (2.4) | 0 (0.0) | 3 (2.9) | 1.220 | 1.122-1.325 |
| BCG | 106 (84.8) | 16 (72.7) | 90 (87.4) | 0.385 | 0.127-1.161 |
| Paciente nuevo | 116 (92.8) | 19 (86.4) | 97 (94.2) | 0.392 | 0.090-1.704 |
| Tiempo de atención > 6 meses | 22 (17.6) | 1 (4.5) | 21 (20.4) | 0.186 | 0.023-1.462 |
| Tiempo al diagnóstico > 6 meses | 23 (18.4) | 2 (9.1) | 21 (20.4) | 0.390 | 0.084-1.804 |
| Localización pulmonar | 47 (37.6) | 7 (31.8) | 40 (38.8) | 0.735 | 0.275-1.959 |
| Localización mixta | 12 (9.6) | 3 (13.6) | 9 (8.7) | 1.649 | 0.408-6.664 |
| Ósea | 3 (2.4) | 1 (4.5) | 2 (1.9) | 2.405 | 0.208-27.75 |
| Miliar | 5 (4.0) | 3 (13.6) | 2 (1.9) | 7.974 | 1.247-50.97 |
| Intestinal/peritoneal | 16 (12.8) | 3 (13.6) | 13 (12.6) | 1.093 | 0.283-4.214 |
| Meníngea/SNC | 12 (9.6) | 5 (22.7) | 7 (6.8) | 4.034 | 1.146-14.19 |
| Genitourinaria | 5 (4.0) | 0 (0.0) | 5 (4.9) | 1.224 | 1.124-1.332 |
| Ganglionar | 25 (20.0) | 1 (4.5) | 24 (23.3) | 0.157 | 0.020-1.226 |
| Inicio del tratamiento | 108 (86.4) | 12 (54.5) | 96 (93.2) | 0.088 | 0.028-0.272 |
| Monorresistencia (resistencia a rifampicina por GenXpert) | 6 (4.8) | 4 (18.2) | 2 (1.9) | 11.222 | 1.911-65.87 |
BCG: Aplicación de la vacuna de Calmette-Guérin. *Para cada variable, los datos representan 125 pacientes.
Las comorbilidades incluyeron hipertensión arterial sistémica (26.4%), diabetes mellitus (21.6%), inmunosupresión iatrogénica (8.8%), artritis reumatoide (8%), desnutrición (8%), trastorno metabólico (7.2%), EPOC (5.6%), VIH (5.6%), depresión (4.8%), neoplasia (4%) y enfermedad renal crónica (2.4%). Otras comorbilidades (0.8% cada una) fueron hepatitis idiopática, anemia, enfermedad de Crohn, espondilitis, fibrosis quística, intolerancia a la glucosa, lupus eritematoso sistémico, linfoma no Hodgkin folicular, síndrome de Down y tromboembolismo pulmonar (Tabla 1).
El seguimiento medio de la cohorte fue de 32 meses (rango: 1-65). Las características clínicas al diagnóstico se resumen en la tabla 1 y los patrones clínicos en la tabla 2 (ambos estratificados según estado vital). Las escalas vitales y de laboratorio aparecen en la tabla 3, y la evolución clínica y complicaciones en la tabla 4.
Tabla 2. Patrón clínico en pacientes con TB atendidos en IMSS Zacatecas (2019-2023)
| Patrón clínico | Defunción | RR | IC 95% | ||
|---|---|---|---|---|---|
| Total (n = 125) Frecuencias (%) | Sí (n = 22) Frecuencias (%) | No (n = 103) Frecuencias (%) | Inferior/Superior | ||
| Convulsiones | 4 (3.2) | 3 (13.6) | 1 (1.0) | 16.105 | 1.589-163.1 |
| Rigidez de nuca | 8 (6.4) | 5 (22.7) | 3 (2.9) | 9.804 | 2.142-44.86 |
| Desorientación | 15 (12.0) | 8 (36.4) | 7 (6.8) | 7.837 | 2.459-24.97 |
| Temblor | 21 (16.8) | 9 (40.9) | 12 (11.7) | 5.250 | 1.852-14.87 |
| Astenia | 91 (72.8) | 20 (90.9) | 71 (68.9) | 4.507 | 0.993-20.44 |
| Letargia | 18 (14.4) | 7 (31.8) | 11 (10.7) | 3.903 | 1.307-11.64 |
| Debilidad muscular | 42 (33.6) | 13 (59.1) | 29 (28.2) | 3.686 | 1.422-9.551 |
| Estupor | 13 (10.4) | 5 (22.7) | 8 (7.8) | 3.493 | 1.020-11.95 |
| Fiebre | 76 (60.8) | 18 (81.8) | 58 (56.3) | 3.491 | 1.104-11.04 |
| Derrame pleural | 9 (7.2) | 2 (9.1) | 7 (6.8) | 3.095 | 0.681-14.05 |
| Somnolencia | 29 (23.2) | 9 (40.9) | 20 (19.4) | 2.873 | 1.078-7.656 |
| Pérdida de peso | 83 (66.4) | 18 (81.8) | 65 (63.1) | 2.631 | 0.828-8.349 |
| Disnea | 19 (15.2) | 6 (27.3) | 13 (12.6) | 2.596 | 0.860-7.829 |
| Tos seca | 75 (60.0) | 16 (72.7) | 59 (57.3) | 2.346 | 0.909-6.047 |
| Hemoptisis | 37 (29.6) | 10 (45.5) | 27 (26.2) | 2.165 | 0.513-9.132 |
| Vómitos | 10 (8.0) | 3 (13.6) | 7 (6.8) | 2.063 | 0.739-5.756 |
| Debilidad | 26 (20.8) | 7 (31.8) | 19 (18.4) | 1.989 | 0.719-5.494 |
| Cefalea | 50 (40.0) | 11 (50.0) | 39 (37.9) | 1.641 | 0.650-4.141 |
| Parálisis | 1 (0.8) | 0 (0.0) | 1 (1.0) | 1.216 | 1.120-1.319 |
| Dolor abdominal | 5 (4.0) | 1 (4.5) | 4 (3.9) | 1.179 | 0.125-11.08 |
| Diaforesis | 59 (47.2) | 11 (50.0) | 48 (46.6) | 1.146 | 0.456-2.878 |
| Adenopatía | 37 (29.6) | 7 (31.8) | 30 (29.1) | 1.044 | 0.209-5.206 |
| Náuseas | 34 (27.2) | 6 (27.3) | 28 (27.2) | 1.004 | 0.357-2.824 |
| Hiporexia | 55 (44.0) | 9 (40.9) | 46 (44.7) | 0.858 | 0.336-2.183 |
| Tos productiva | 50 (40.0) | 8 (36.4) | 42 (40.8) | 0.830 | 0.319-2.153 |
| Otros | 21 (16.8) | 1 (4.5) | 20 (19.4) | 0.198 | 0.025-1.557 |
Para cada variable, los datos representan 125 pacientes.
Tabla 3. Escalas vitales y de laboratorio en pacientes con TB atendidos en IMSS Zacatecas (2019-2023)
| Escala | Puntuación | Media (DE) |
|---|---|---|
| FR | – | 19.9 (3.3) |
| TAM | – | 113.6 (17.8) |
| Leucocitos (×1000) | – | 8 (4.4) |
| Linfocitos (×1000), promedio | – | 4.8 (8.2) |
| Neutrófilos | – | 20.1 (2.8) |
| Hb | – | 12.6 (2.6) |
| Plaquetas | – | 326 (110) |
| Eritrocitos | – | 4.5 (0.8) |
| TGO | – | 45.3 (5.8) |
| TGP | – | 30.3 (12.9) |
| Colesterol | – | 177.6 (106.2) |
| LAD | – | 43.3 (14.6) |
| Creatinina | – | 1.1 (1.4) |
| Urea | – | 40.5 (34.5) |
| INL | – | 6.9 (7.7) |
| Glasgow | – | 15 (2.1) |
| QSOFA | 0 | 107 (85.6%) |
| 1 | 8 (6.4%) | |
| 2 | 2 (1.6%) |
FR: frecuencia respiratoria; Hb: hemoglobina; INL: índice neutrófilo/linfocito; LAD: lipoproteína de alta densidad; QSOFA: evaluación rápida de disfunción orgánica por sepsis (QSOFA 2-3); TAM: tensión arterial media; TGP: transaminasa glutámico-oxalacética; TGP: transaminasa glutámico-pirúvica.
Tabla 4. Evolución clínica de los pacientes con TB en el IMSS en Zacatecas (2019-2023)
| Patología | Subpatología | n (%) |
|---|---|---|
| Complicaciones | – | 61 (48.8%) |
| Complicaciones inmunológicas | – | 3 (2.4%) |
| Complicaciones urogenitales | – | 4 (3.2%) |
| Complicaciones cardíacas | – | 1 (0.8%) |
| Complicaciones GI | – | 17 (13.6%) |
| Complicaciones respiratorias | – | 17 (13.6%) |
| Complicaciones del SNC | Signos motores | 11 (8.8%) |
| Oclusión de la vena central de la retina del ojo izquierdo | 1 (0.8%) | |
| Paraparesia flácida | 1 (0.8%) | |
| Psicosis | 1 (0.8%) | |
| Vasculitis del SNC / hemiplejia | 1 (0.8%) | |
| LRA | – | 21 (16.8%) |
| Choque séptico | – | 10 (8%) |
| Derrame pleural | – | 8 (6.4%) |
| Defunción | – | 22 (17.6%) |
GI: gastrointestinal; LRA: lesión renal aguda; SNC: sistema nervioso central.
Los hallazgos radiográficos torácicos más comunes fueron patrón miliar (16%), fibrosis pulmonar (7.3%), consolidación (7.4%), cavitación (6.4%), nódulos pulmonares (3.2%), tuberculoma (2.4%) y atelectasia (1.6%); neumotórax, bronquiectasias, empiema y bulas representaron cada uno 0.8%. La tomografía computarizada (TC) se realizó en el 12%de los pacientes; los patrones característicos incluyeron consolidación (1.6%), opacidades en vidrio deslustrado (1.6%), cavitación y patrón en “árbol en brote” (2.4%), patrón miliar (1.6%) y nódulos (1.6%).
La tasa de mortalidad de la cohorte fue de 17.6% (Tabla 4).
Factores de riesgo asociados a la muerte
(RR = 5.6; IC 95%, 2.124-15.11), alcoholismo (RR = 3.6; IC 95%, 1.289-10.23), antecedente de TB (RR = 1.2; IC 95%, 1.126-1.336) y contacto con un caso de TB (RR = 1.22; IC 95%, 1.123-1.329) (Tabla 1).
Las comorbilidades y tratamientos asociados a un mayor riesgo de muerte fueron enfermedad renal crónica (RR = 1.22; IC 95%, 1.122-1.325), desnutrición (RR = 5.7; IC 95%, 1.506-22.06), neoplasia (RR = 1.22; IC 95%, 1.124-1.332), trastorno metabólico (RR = 1.23; IC 95%, 1.130-1.347) y hemodiálisis (RR = 1.22; IC 95%, 1122-1.325) (Tabla 1).
Los factores diagnósticos asociados al riesgo de muerte fueron localización miliar (RR = 7.9; IC 95%, 1.247-50.97), localización meníngea/SNC (RR = 4.03; IC 95%, 1.146-14.19) y Mycobacterium tuberculosis resistente a rifampicina (RR = 11.22; IC 95%, 1.911-65.87) (Tabla 1).
Los signos clínicos asociados a la muerte incluyeron convulsiones (RR = 16.1; IC 95%, 1.589-163.1), rigidez de nuca (RR = 9.8; IC 95%, 2.142-44.86), desorientación (RR = 7.8; IC 95%, 2.459-24.97), temblor (RR = 5.25; IC 95%, 1.85-14.87), letargo (RR = 3.90; IC 95%, 1.30-11.64), debilidad muscular (RR = 3.68; IC 95%, 1.42-9.55), fiebre (RR = 3.49; IC 95%, 1.10-11.04), estupor (RR = 3.49; IC 95%, 1.02-11.95), somnolencia (RR = 2.87; IC 95%, 1.07-7.65) y parálisis (RR = 1.21; IC 95%, 1.120-1.319) (Tabla 2).
Los hallazgos radiológicos asociados a un mayor riesgo de muerte fueron neumotórax (RR = 6.1; IC 95%, 4.08-9.10), bronquiectasias (RR = 5.9; IC 95%, 3.99-8.71), empiema (RR = 5.9; IC 95%, 3.99-8.71), consolidación (RR = 4.51; IC 95%, 1.10-18.54), patrón miliar (RR = 4.33; IC 95%, 1.50-12.46), nódulos pulmonares (RR = 1.22; IC 95%, 1.12-1.32), tuberculoma (RR = 1.22; IC 95%, 1.122-1.32), atelectasia (RR = 1.21; IC 95%, 1.12-1.32) y bulas (RR = 1.21; IC 95%, 1.12-1.31).
Los índices de gravedad y complicaciones asociados a un mayor riesgo de muerte incluyeron INL ≥ 10 (RR = 10.44; IC 95%, 3.54-30.75), Quick Sepsis Organ Failure Assessment (qSOFA 2-3) (RR = 6.15; IC 95%, 4.11-9.18), cualquier complicación (RR 15.12; IC 95%, 3.35-68.18), complicaciones gastrointestinales (RR = 4.34; IC 95%, 1.43-13.15), complicaciones respiratorias (RR = 4.34; IC 95%, 1.43-13.15) y lesión renal aguda (RR = 3.95; IC 95%, 1.39-11.25).
Análisis de supervivencia
La regresión logística por pasos identificó variables independientes de riesgo de muerte: M. tuberculosis resistente a rifampicina (RR 141.31; IC 95%, 8.75-2280. 86; p = 0), convulsiones (RR 132.31; IC 95%, 7.61-2299. 87; p = 0.001), INL ≥ 10 puntos al diagnóstico (RR 47.68; IC 95%, 8.04-282.68; p = 0), TB miliar (RR 16.14; IC 95%, 1.048-248.74; p = 0.046) y alcoholismo (RR 8.74; IC 95%, 1.4-54.50; p = 0.020).
El análisis de Kaplan-Meier mostró una supervivencia del 74.3% a los 32 meses para toda la cohorte (Material suplementario, figura 1). Los modelos de regresión de Cox calcularon la supervivencia para los factores de riesgo significativos (Figura 1): entre los casos resistentes a rifampicina, el 33% presentó un tiempo de supervivencia < 20 meses vs 76.67% de supervivencia a cinco años en los casos susceptibles (p < 0.001). Para INL ≥ 10, el 17% presentó supervivencia < 40 meses vs 85.46% de supervivencia más allá de 60 meses en quienes no tenían INL elevado (p < 0.001). Entre aquellos pacientes con TB miliar, el 30% tuvo supervivencia < 20 meses vs 76.13% con supervivencia más allá de 60 meses en los casos no miliares (p = 0.046). En el grupo de pacientes con consumo de alcohol, el 57.7% presentó supervivencia de 30 meses vs 78.31% con supervivencia más allá de 60 meses en quienes no consumían alcohol (p = 0.020). El modelo de Cox completo se detalla en el material adicional.
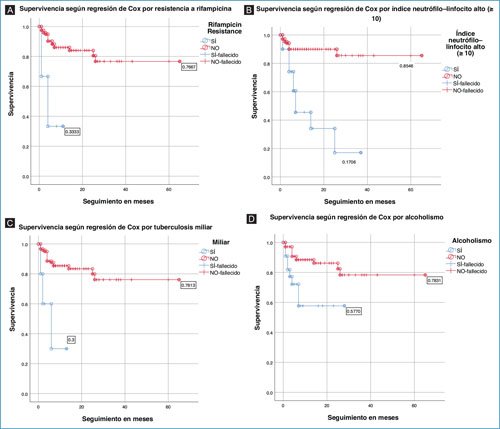
Figura 1. Modelo de regresión de Cox. Estimación de supervivencia según los factores de riesgo identificados en la regresión logística. Se muestra el efecto de cada variable sobre la mortalidad. A: resistencia a rifampicina B: INL alto C: localización miliar D: alcoholismo. Utilizando valores de corte de 60 meses de evolución, se representa el porcentaje de casos que sobreviven en cada escenario comparativo.
Discusión
A pesar de los avances en el control de la TB, se estima que 8 millones de personas desarrollan TB anualmente y casi 2 millones fallecen5. Aproximadamente una cuarta parte de la población mundial está infectada por Mycobacterium tuberculosis, y entre 5-10% desarrolla enfermedad activa a lo largo de su vida; el riesgo de reactivación está fuertemente influenciado por el estado inmunológico.
Tal y como se muestra en el presente trabajo, las características epidemiológicas de la TB en Zacatecas reflejan patrones nacionales y globales: la desnutrición, el envejecimiento, la diabetes, los trastornos por consumo de alcohol y el tabaquismo aumentan la progresión de TB de forma independiente o como comorbilidades6–9. México ocupa el tercer lugar en América Latina en TB pulmonar y extrapulmonar (TBEP). El grupo etario más afectado se ubica entre 15-45 años, con mayor mortalidad en adultos mayores y riesgo adicional asociado con comorbilidades10–11. Series hospitalarias en México reportan predominio de TB pulmonar, coinfección frecuente por VIH en algunos entornos y TB meníngea entre las manifestaciones extrapulmonares12–14. En cambio, nuestra cohorte incluyó 37% de TB pulmonar, con formas extrapulmonares descendiendo en prevalencia entre afectación ganglionar, intestinal, meníngea/SNC, genitourinaria y miliar.
La resistencia farmacológica detectó en el 4,8% de los casos, valor inferior al descrito en otras regiones de México6,15. Las comorbilidades en esta cohorte incluyeron la hipertensión arterial sistémica como la más frecuente, seguida de diabetes y otras; la prevalencia de diabetes (21.6%) y el VIH (5.6%) fue parecido al descrito en reportes externos. La comorbilidad tuberculosis-diabetes parece más prevalente que TB-VIH en nuestro entorno, conforme a tendencias globales16.
Los factores demográficos y conductuales vinculados a la muerte incluyeron hacinamiento, alcoholismo y tabaquismo, concordantes con la evidencia que indica que el tabaco y el alcohol incrementan el riesgo de recurrencia, recaída y mortalidad durante el tratamiento, con efectos sinérgicos adversos17,18.
La desnutrición duplicó al menos el riesgo de muerte, lo cual coincide con lo descrito en la literatura médica que asocia la desnutrición a incrementos de mortalidad de 2 a 4 veces en TB19. Nuestro análisis de supervivencia mostró riesgo elevado con alcoholismo, NLR ≥ 10 al diagnóstico, TB miliar y resistencia a rifampicina; las convulsiones estuvieron cerca de significación en los modelos de supervivencia.
Coincidiendo con nuestro estudio, en Tamaulipas (noreste de México), un análisis multivariado mostró que en adultos mayores (≥ 65 años), comparados con jóvenes (18-39 años) y adultos de mediana edad (40-64 años), el consumo excesivo de alcohol aumentó el riesgo de muerte durante el tratamiento anti-TB20. Según tasas de mortalidad post-tratamiento de TB (2008-2019) en Georgia (Estados Unidos), el análisis multivariado reportó un aumento del riesgo de mortalidad asociado con consumo excesivo de alcohol21. Un metanálisis muestra que el consumo de alcohol incrementa el riesgo de fracaso terapéutico y muerte tanto en TB sensible como en TB multirresistente22.
El INL (índice neutrófilo-linfocito) se utiliza para la vigilancia, estratificación y pronóstico de diversos síndromes clínicos y enfermedades. Como un sustituto común de inflamación y estrés, integra la función inmunológica, endocrina y del sistema nervioso autónomo. Un metanálisis propuso el INL para discriminar entre TB y neumonía bacteriana adquirida en la comunidad, dado que los pacientes con TB presentaron niveles más bajos23. En la TB pulmonar sensible a rifampicina recién diagnosticada, el INL disminuyó en aquellos pacientes que respondieron al tratamiento farmacológico (esputo negativo en 2 meses). Los autores propusieron este índice/ratio como herramienta para monitorizar la respuesta al tratamiento24. En el presente trabajo, por primera vez se reporta que un INL ≥ 10 se asocia con un mayor riesgo de muerte por TB.
La TB del sistema nervioso central (SNC) conlleva una elevada morbimortalidad; sus signos clínicos pueden ser inespecíficas e incluir convulsiones e hidrocefalia. La TB miliar refleja diseminación hematógena con afectación pulmonar y extrapulmonar simultánea y alto riesgo de meningitis tuberculosa25–30. Según nuestros hallazgos, es plausible la TB del SNC esté infradiagnosticada: entre los pacientes con convulsiones al diagnóstico, las formas meníngea y miliar estuvieron presentes y se asociaron a muerte en varios casos.
A nivel mundial, la TB resistente a rifampicina y la TB resistente a varios fármacos siguen siendo factores que contribuyen significativamente a la mortalidad31. México se encuentra entre los 5 países con mayor número de casos de TB y TB-MDR en América Latina. El riesgo observado en nuestra cohorte asociado a la resistencia a la rifampicina fue alto, sin evidencia clara de agrupamiento con comorbilidades específicas, lo que subraya la necesidad de una identificación rápida y el inicio oportuno del tratamiento adecuado.
Conclusiones
Los factores epidemiológicos asociados a la TB en Zacatecas reflejan los patrones nacionales, con una mayor frecuencia de la TBEP. El riesgo de muerte aumentó en pacientes con alcoholismo, INL ≥ 10 al diagnóstico, TB miliar y resistencia a rifampicina. Estos hallazgos enfatizan la importancia de brindar asesoramiento sobre el consumo de alcohol y reforzar la adherencia a la terapia antimicrobiana.
El INL podría ser útil como predictor de desenlaces adversos en TB, complementando su rendimiento diagnóstico previamente descrito como biomarcador de vigilancia y seguimiento terapéuticos.
Dado el posible infradiagnóstico de la TB meníngea, debería tenerse en cuenta realizar evaluaciones sistemáticas del SNC ante la presencia de TB miliar, utilizando PCR o secuenciación de alto rendimiento en líquido cefalorraquídeo cuando sea posible.
Identificar los factores de riesgo asociados a una menor supervivencia proporciona una base para desarrollar estrategias preventivas destinadas a mejorar la supervivencia de pacientes con TB.
Financiamiento
Ninguna agencia financiadora participó en el diseño del estudio, la recolección y análisis de datos, la decisión de publicar ni la preparación del manuscrito.
Conflicto de intereses
Los autores declaran que no existen intereses financieros ni personales que pudieran haber influido en el trabajo presentado en este artículo.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han obtenido la aprobación del Comité de Ética para el análisis de datos clínicos obtenidos de forma rutinaria y anonimizados, por lo que no fue necesario el consentimiento informado. Se han seguido las recomendaciones pertinentes.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
